- История
- Происхождение названия
- Нахождение в природе
- Важнейшие соединения:
- Электронная схема ртути
- Степень окисления ртути
- Молярная масса ртути
- Валентность Hg
- Квантовые числа Hg
- Физические свойства
- Химические особенности
- Технология получения
- Процесс производства ртути из руды
- Хранение и транспортировка
- Месторождения, добыча
- Присутствие в природе
- Где находит применение ртуть
- Ртутные приборы
- Электрический аккумулятор
- Люминесцентные и кварцевые лампы
- Термометры
- Меры предосторожности при обращении с ртутным градусником
- Утилизация ртути: что делать с разбитым градусником?
- Как собрать ртуть с помощью магнита?
- Утилизация ртутьсодержащих отходов
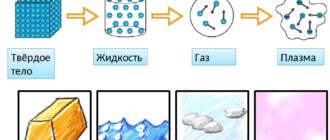
История
Ртуть — один из семи металлов, известных с древнейших времён. Нередко её находили в самородном виде (жидкие капли на горных породах), но чаще получали обжигом ее основного минерала — киновари. Киноварная краска применялась на территории современной Турции с 8 тыс. до н. э., киноварные месторождения юго-восточных провинций современного Китая разрабатывались с 4 тыс. до н. В древнем Египте киноварь и металлическую ртуть использовали с 3-го тысячелетия до н. э., в древней Индии — с 1-2 тысячелетий до н. э. В Египте был найден сосуд с ртутью, датированный XV—XVI вв. до н. э. В Египте, Месопотамии и Китае был известен способ получения ртути из киновари при помощи меди и уксуса. В VII в. до н. э. ассирийские ремесленники применяли ртуть для золочения металлических поверхностей (амальгамирование). Aмальгамирование было известно древним грекам и римлянам, они знали и о токсичности самой ртути и её соединений, в частности сулемы. Ртуть и киноварь упоминаются в «Естественной истории» Плиния Старшего.
Много веков алхимики считали ртуть главной составной частью всех металлов и полагали, что если жидкой ртути возвратить твёрдость при помощи серы или мышьяка, то получится золото. Выделение ртути в чистом виде было описано шведским химиком Георгом Брандтом в 1735 году. Для представления элемента как у алхимиков, так и в настоящее время используется символ планеты Меркурий. Твердая ртуть впервые была получена российскими учеными Ломоносовым и Брауном, которые в декабре 1759 года смогли заморозить ртуть и установить её металлические свойства в твёрдом состоянии: ковкость, электропроводность и др.; было показано, что ртуть и в жидком, и в твердом состоянии проводит электрический ток.
Происхождение названия
Русское название ртути, по одной из версий, — это заимствование из арабского (через тюркские языки); по другой версии, «ртуть» связана с литовским ritu — качу, катаю, происшедшим от индоевропейского рет (х) — бежать, катиться.
Нахождение в природе
Ртуть — относительно редкий элемент в земной коре со средней концентрацией 83 мг/т. Однако ввиду того, что ртуть слабо связывается химически с наиболее распространёнными в земной коре элементами, ртутные руды могут быть очень концентрированными по сравнению с обычными породами. Наиболее богатые ртутью руды содержат до 2,5 % ртути. Основная форма нахождения ртути в природе — рассеянная, и только 0,02 % её заключено в месторождениях. Содержание ртути в различных типах изверженных пород близки между собой (около 100 мг/т). Из осадочных пород максимальные концентрации ртути установлены в глинистых сланцах (до 200 мг/т). В водах Мирового океана содержание ртути — 0,1 мкг/л. Важнейшей геохимической особенностью ртути является то, что среди других халькофильных элементов она обладает самым высоким потенциалом ионизации. Это определяет такие свойства ртути, как способность восстанавливаться до атомарной формы (самородной ртути), значительную химическую стойкость к кислороду и кислотам.
Ртуть присутствует в большинстве сульфидных минералов. Особенно высокие её содержания (до тысячных и сотых долей процента) устанавливаются в блёклых рудах, антимонитах, сфалеритах и реальгарах. Близость ионных радиусов двухвалентной ртути и кальция, одновалентной ртути и бария определяет их изоморфизм во флюоритах и баритах. В киновари и метациннабарите сера иногда замещается селеном или теллуром; содержание селена часто составляет сотые и десятые доли процента. Известны крайне редкие селениды ртути — тиманит (HgSe) и онофрит (смесь тиманита и сфалерита).
Ртуть является одним из наиболее чувствительных индикаторов скрытого оруденения не только ртутных, но и различных сульфидных месторождений, поэтому ореолы ртути обычно выявляются над всеми скрытыми сульфидными залежами и вдоль дорудных разрывных нарушений. Эта особенность, а также незначительное содержание ртути в породах, объясняются высокой упругостью паров ртути, возрастающей с увеличением температуры и определяющей высокую миграцию этого элемента в газовой фазе.

В обычных условиях киноварь и металлическая ртуть не растворимы в воде, но в присутствии некоторых веществ (Fe2(SO4)3, озон, пероксид водорода) растворимость в воде этих минералов достигает десятков мг/л. Особенно хорошо растворяется ртуть в сульфидах щелочных металлов с образованием, например, комплекса HgS•nNa2S. Ртуть легко сорбируется глинами, гидроксидами железа и марганца, глинистыми сланцами и углями.
В природе известно около 20 минералов ртути, но главное промышленное значение имеет киноварь HgS (86,2 % Hg). В редких случаях предметом добычи является самородная ртуть, метациннабарит HgS и блёклая руда — шватцит (до 17 % Hg). На единственном месторождении Гуитцуко (Мексика) главным рудным минералом является ливингстонит HgSb4S7. В зоне окисления ртутных месторождений образуются вторичные минералы ртути. К ним относятся, прежде всего, самородная ртуть, реже метациннабарит, отличающиеся от таких же первичных минералов большей чистотой состава. Относительно распространена каломель Hg2Cl2. На месторождении Терлингуа (Техас) распространены и другие гипергенные галоидные соединения — терлингуаит Hg2ClO, эглестонит Hg6Cl4O (по другим данным Hg6OCl3(OH), Hg6HCl3O2 ).
Важнейшие соединения:
Соединения ртути(I) в большинстве неустойчивы, легко окисляются, восстанавливаются и диспропорционируют:
- Оксид ртути(I), Hg2O, черный порошок, неустойчив, легко разлагается под действ. тепла или света, не растворим.
- Нитрат ртути(I), Hg2(NO3)2, бесцветные кристаллы, растворим, гидролизуется по катиону.
- Сульфат ртути(I), Hg2SO4, желто-белые кристаллы, нерастворим, образует кристаллогидрат Hg2SO4*2H2O.
- Хлорид ртути(I), «каломель», Hg2Cl2 — бесцветные кристаллы, нерастворим.
- Оксид ртути(II), HgO, существует в красной или желтой модификации, основной оксид, растворяясь в кислотах образует соли ртути(II), с водой не реагирует. При нагревании выше 300°C разлагается.
- Нитрат ртути(II), Hg(NO3)2, бесцветные кристаллы, растворим, гидролизуется по катиону.
- Хлорид ртути(II), «сулема», HgCl2 — бесцветные кристаллы, хорошо растворим.
- ртути(II), HgI2 — ярко-красное вещество, нерастворимо в воде, но растворимо в избытке раствора KI? образуя комплексное соединение: HgI2 + 2KI = K2[HgI4].Щелочной раствор этого комплексного соединения используется в аналитической химии для обнаружения аммиака и ионов аммония («реактив Несслера»): K2[HgI4] + NH3 + 3KOH = [Hg2N]I*H2O + 7 KI + 2H2O (образуется желтый осадок)
Электронная схема ртути
Hg: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10
Короткая запись:
Hg: [Xe]6s2 4f14 5d10
Одинаковую электронную конфигурацию имеют атом ртути и +1Tl, +2Pb, +3Bi, +4Po, +5At
Порядок заполнения оболочек атома ртути (Hg) электронами: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s → 4f → 5d → 6p → 7s → 5f → 6d → 7p.
На подуровне ‘s’ может находиться до 2 электронов, на ‘s’ — до 6, на ‘d’ — до 10 и на ‘f’ до 14
Ртуть имеет 80 электронов, заполним электронные оболочки в описанном выше порядке:
2 электрона на 1s-подуровне
2 электрона на 2s-подуровне
6 электронов на 2p-подуровне
2 электрона на 3s-подуровне
6 электронов на 3p-подуровне
2 электрона на 4s-подуровне
10 электронов на 3d-подуровне
6 электронов на 4p-подуровне
2 электрона на 5s-подуровне
10 электронов на 4d-подуровне
6 электронов на 5p-подуровне
2 электрона на 6s-подуровне
14 электронов на 4f-подуровне
10 электронов на 5d-подуровне
Степень окисления ртути
Атомы ртути в соединениях имеют степени окисления 2, 1.
Степень окисления — это условный заряд атома в соединении: связь в молекуле между атомами основана на разделении электронов, таким образом, если у атома виртуально увеличивается заряд, то степень окисления отрицательная (электроны несут отрицательный заряд), если заряд уменьшается, то степень окисления положительная.
Молярная масса ртути
Ртуть – химический элемент, расположенный в шестом периоде во IIВ группе Периодической таблицы Д.И. Менделеева.
Порядковый номер – 80. Строение атома показано на рис. 1. Металл d-семейства.
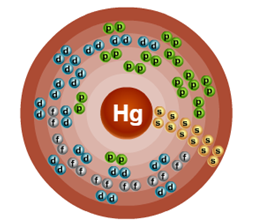
Рис. 1. Схема строения атома ртути.
В обычных условиях ртуть представляет собой единственный металл, находящийся при комнатной температуре в жидком состоянии. В виде простого вещества ртуть представляет собой серебристо-белый металл. Очень легкоплавкий металл. Плотность 13,55 г/см3. Температура плавления — 38,9oС, кипения 357oС.
Молярная масса ртути равна 200,59 г/моль. Данное значение показывает отношение массы вещества (m) е число моль данного вещества (n), обозначается M и может быть рассчитано по формуле:
M = m / n.
Иными словами, молярная масса вещества – это масса 1 моль данного вещества, выраженная в г/моль или ккмоль.
Ртуть не может существовать в виде газа, только в форме твердого вещества, поэтому для нахождения значения его молярной массы нельзя использовать величину молярного объема или производить расчеты по формуле Менделеева-Клапейрона.
Валентность Hg
Атомы ртути в соединениях проявляют валентность II, I.
Валентность ртути характеризует способность атома Hg к образованию хмических связей. Валентность следует из строения электронной оболочки атома, электроны, участвующие в образовании химических соединений называются валентными электронами. Более обширное определение валентности это:
Число химических связей, которыми данный атом соединён с другими атомами
Валентность не имеет знака.
Квантовые числа Hg

Физические свойства

Металлическая ртуть

Переливание ртути из сосуда в сосуд
Электронная оболочка атома ртути обладает заполненными электронными подуровнями, последние из которых — 4f14 5d10 6s2. Главное отличие ртути от двух других металлов с аналогичной структурой электронного облака, цинка (3d 4s) и кадмия (4d 5s) — заполненность f-подуровня, находящегося по энергии ниже 6s-подуровня. Орбитали f-электронов имеют сложную форму и большой размер, они плохо экранируют заряд ядра. Поэтому удерживающие силы, действующие на 6s-электроны, относительно велики, и 6s-подуровень намного более стабилен, чем у любых других металлов. Этим обусловлены уникальные физические и химические свойства ртути. Так, ртуть — единственный металл, который находится в жидком состоянии при комнатной температуре. Температура плавления составляет 234,32 K (−38,83 °C), кипит при 629,88 K (356,73 °C), критическая точка — 1750 K (1477 °C), 152 МПа (1500 атм). Обладает свойствами диамагнетика. Образует со многими металлами жидкие и твёрдые сплавы — амальгамы. Стойкие к амальгамированию металлы: V, Fe, Mo, Cs, Nb, Ta, W, Co.
Плотность ртути при нормальных условиях — 13 596 кг/м³.
Химические особенности
Металл характеризуется степенью окисления +1 и +2. В первом случае он представлен двухъядерным катионом Hg22+ с металлической связью и склонен к диспропорционированию, которое проходит при нагревании и разбавлении водой.
На холоде вещество со степенью окисления +2 и металлическая ртуть сопропорционируют. Реагируя с нитратом металла, элемент образует нитрат ртути. При степени окисления +2 получаются катионы Hg2+, которые легко гидролизуются. Гидроксид металла существует лишь в разбавленных растворах, а в жидкостях с высокой концентрацией он дегидратируется.
Элемент со степенью окисления +2 образует с различными лигандами устойчивые комплексы. Прочные ковалентные связи наблюдаются с йодом, серой и углеродом. С последним веществом ртуть образует самые устойчивые соединения.
Технология получения
Способы получения ртути не изменились со времен Средневековья. На предприятиях все так же обжигают киноварь (то есть сульфид ртути).
- Вещество нагревают, получающиеся пары превращают в конденсат, собирают.
- Второй метод – металлотермический. То есть восстановление чистой ртути другими металлами при повышенных температурах.
Процесс производства ртути из руды
Технология получения ртути из измельчённой руды, состоит из нескольких этапов:
- Обжиг. Мелкоизмельчённая руда нагревается в трубчатой печи до определённой температуры. В результате химического взаимодействия с кислородом, образуется диоксид серы и происходит испарение ртути.
- Конденсация. Получившаяся после обжига газообразная смесь, содержащая в себе ртутные испарения, двуокись серы, водяной пары и другие побочные вещества, попадает в конденсатор охлаждения. Где сама ртуть конденсируется в жидкое состояние, а оставшиеся газы и пары или находят дальнейшее применение, или выбрасываются в атмосферу.
- Консолидация и очистка. В специально определённой ёмкости ртуть накапливается и очищается от примесей, оставшихся на её поверхности. Такое становится возможным благодаря очень высокой плотности перерабатываемого минерала.
- Доочистка. Так как полученный продукт не всегда удовлетворяет требованиям последующего использования, то осуществляется трёхступенчатая доочистка, включающая:
- механическую фильтрацию,
- электролиз,
- химическую очистку активными компонентами.
Конечным результатом этих процессов выступает пригодная для дальнейшего использования ртуть, находящее применение в ряде отраслей народного хозяйства.
Хранение и транспортировка
Так как ртуть и её целый ряд химических соединений, имеющих её в своём составе, представляют угрозу для жизни и здоровья, то хранение и перевозка этого вещества чрезвычайной опасности должна производиться специально обученными лицами в предназначенной для этой процедуры таре.
Складское хранение и транспортировка ртути разрешена только в баллонах, изготовленных из чёрной стали, плотно закрывающихся снаружи и эмалированных внутри. Допускается нахождение ртути в толстостенных стеклянных ёмкостях с притёртыми пробками на рабочих местах в необходимых объёмах. Причём поверхность жидкого металла должна быть залита водой или глицерином с целью недопущения испарения вредных паров. Емкости должны располагаться на подносах внутри вытяжных шкафов. Места хранения, проведения погрузочно-разгрузочных работ и расфасовки должны быть оборудованы специальными приспособлениями и посудой.
Транспортировка этого опасного вещества должна осуществляться исключительно в небьющейся посуде. Транспорт для перевозки необходимо иметь в исправном состоянии, а водители – обладать соответствующими допусками и разрешениями.
Месторождения, добыча
Ртутные месторождения планеты исчисляются поштучно:
- Крупнейшими залежами располагает Испания.
- Запасы руды разведаны на Кавказе, Памире, Европе (Словения, Украина).
- В России зарегистрировано более двадцати месторождений, крупнейшие – на Чукотке. Национальные запасы оцениваются в 15,6 тыс. тонн.
Словенский город Идрия — крупнейший в Европе центр добычи ртути с XV века
В природе выявлено два десятка ртутных минералов, однако промышленный интерес представляет только киноварь (сульфид с содержанием ртути 86%). Иногда рентабельна добыча самородной ртути и шватцита (до 17%).
Мировая цена ртути разной степени очистки – $30-100 за кг.
Присутствие в природе
Почти всегда вещество представлено в виде руды. Самые богатые ртутные руды содержат до 2,5% ртути.
Наиболее богаты ртутью породы осадочного происхождения (особенно глинистые сланцы) – до 200 мг/т. Вдвое беднее продукты вулканизма.
Каждая тонна земной коры содержит 0,83 г ртути. Каждый литр вод Мирового океана – 0,1 мкг.
Пары ртути ядовиты. Их выброс в атмосферу – «заслуга» вулканов и человека в равной мере. Люди создают такие осадки, эксплуатируя ТЭЦ, добывая золото, выплавляя цветные металлы, производя цемент, соду, утилизируя мусор.
Где находит применение ртуть
Уникальные свойства сделали ртуть в современных отраслях промышленности важным элементом. Нет такой отрасли, где бы не использовался этот необычный металл:
Химическая промышленность:
- самое массовое потребление ртути используется в хлорном производстве, она является катодом в электролитическом процессе получения едкого натрия и хлора;
- в качестве катализатора при образовании органических соединений;
- для растворения урановых блоков, используемых в атомной энергетике.
- при термохимической реакции разложения воды на кислород и водород в атомно-водородной энергетике.
Металлургия:
- использует свойство ртути растворять в себе большинство металлов, в результате чего получаются амальгамы;
- целый ряд важнейших сплавов получается с помощью ртути, находящих применение в гальванопластике, гравировке и литографии;
- ртутные соединения применяют в производстве драгоценных металлов.
Тяжёлое машиностроение:
- вакуумные установки;
- современны ртутные диффузионные насосы;
- тяжелонагруженные гидродинамические подшипники;
- ртутнопаровые турбины содержат большое количество ртути в жидком состоянии и его необходимо постоянно пополнять.
Электротехническая промышленность:
- лампы дневного света, кварцевые, люминесцентные;
- выпрямители электрического тока, преобразующие трёхфазный ток в постоянный посредством жидкого ртутного катода;
- сухие батареи, технология изготовления которых включает применение ртути, сегодня на них работают слуховые аппараты;
- аккумуляторы.
Приборостроение и радиотехническая промышленность:
- контрольно-измерительные приборы (манометры, ареометры, барометры, термометры), полярографы;
- ртутные муфты входят в сборку миниатюрных двигателей для стиральных машин, холодильников, кондиционеров;
- в астрономии есть ртутный прибор — горизонт, где металл выступает в роли идеальной зеркальной поверхности для наблюдения за небесными телами.
В горном деле ртуть помогает отделить от золота неметаллические примеси.
Нефтеперерабатывающая промышленность использует способность ртутных паров к точной регулировке температур при очистке нефти.
Военная промышленность из ртути и её соединений получает «гремучую ртуть» — взрывчатое вещество, закладываемое в детонаторы снарядов и гранат.
Медицина получает антисептические, противопаразитарные, мочегонные препараты ртути. Стоматология изготавливает зубные протезы и пломбы из амальгамы олова, серебра и кадмия.

Сельское хозяйство применяет органические соединения ртути как гербициды и для протравливания семян.
В судостроении подводную часть морских судов покрывают специальной краской, содержащей ртуть. Соединяясь с морским хлором, на покрытии днища образуется сулема, от которой вредные бактерии гибнут.
Органические и неорганические соединения ртути находят применения в фотографии, пиротехнике, при изготовлении художественных изделий из фарфора, дублении кожи, окрашивании тканей.
Ртутные приборы
Физико-химические свойства являются главной причиной, по которой происходит применение ртути в разных приборах и машинах. Пары металла используются в ртутных турбинах. Такие установки особенно выгодны, когда в агрегате мало воды и охлаждение механизма происходит исключительно воздухом.
В электротехнике применяют выпрямители с жидким ртутным катодом. Они позволяют преобразовать трехфазный электрический ток в постоянный. Даже в астрономических целях применяют ртутные приборы – горизонты. Они имеют специальный сосуд с жидким металлом, поверхность которого служит зеркалом во время наблюдений за космосом. Также применение ртути в современной промышленности проявляется в производстве разных диффузионных насосов, прерывателей, термометров.
Во многих отраслях медицины используют ртутно-кварцевые лампы, которые облучают ультрафиолетовыми лучами. Также незаменимым медицинским инструментом является всем известный градусник для измерения температуры тела.
Электрический аккумулятор
В электрическом аккумуляторе благодаря обратимости химических реакции происходит накопление энергии. Это позволяет использовать их как автономный (резервный) источник тока. Эксплуатационные характеристики зависят от типа электролита и состава электродов.
В ртутных аккумуляторах электролитом является ртуть. Они обладают высокой энергоемкостью, энергоплотностью, поддерживают постоянное напряжение. Но так как стоимость ртути высокая и она токсична, их практически не выпускают.
Люминесцентные и кварцевые лампы
Эти лампы представляют собой источник света низкого давления. В обеих лампах электрический разряд проходит через смесь инертного газа и ртутных паров, образуя ультрафиолет.
В люминесцентных лампах герметичная колба, заполненная ртутной смесью, покрыта изнутри люминоформом. Это сделано для того, чтобы перевести невидимое ультрафиолетовое излучение в видимое.
От состава люминоформа получают свет теплого или холодного спектра. Люминесцентные по своей светоотдаче намного эффективнее обыкновенных ламп накаливания, потребляют меньше электроэнергии.
В кварцевых лампах нет люминофоромного покрытия, а колба выполнена из кварцевого стекла. Благодаря этому ультрафиолет попадает напрямую в помещение и дезинфицирует комнату. Воздух в помещении становится стерильным, микробы погибают.
Термометры
Ртуть изменяет объем в зависимости от температуры. При повышении она увеличивается, при снижении температуры уменьшается соответственно. На этом свойстве и основан принцип работы термометра. Трубочка со ртутью помещается на шкалу с делениями, по которой измеряется температура.
Меры предосторожности при обращении с ртутным градусником
Каждый взрослый так или иначе умеет обращаться с ртутным градусником. Сложного в этом ничего нет. Но самое главное – он должен храниться в отдельном месте и как можно дальше от детей. Также неплохо, если градусник находится в собственном футляре.

Утилизация ртути: что делать с разбитым градусником?
Об утилизации разбитого градусника нужно знать следующее:
- Нельзя просто выбросить градусник вместе с другими домашними отходами.
- Не пытайтесь пропылесосить или подмести ртутные шарики веником. Пылесос придется сразу же выбросить из-за этого, ведь вы облегчили испарение ртути. А веник способен размельчить шарики на мельчайшие частицы, но вреда от них потом будет не меньше.
- Нельзя смывать в туалет. Остатки ртути осядут на трубах, а вот извлечь ее оттуда будет крайне сложно, практически невозможно.
- Лучше не делать попыток самостоятельно утилизировать градусник. То есть закапывать его где-либо, выбрасывать в реку или хранить где-то. Этим занимаются специально подготовленные специалисты.
- Одежду, в которой вы были, когда убирали остатки градусника лучше выбросить, но если это невозможно, то хотя бы не стирайте ее в стиральной машинке вместе с другими вещами.
О ближайшем пункте сбора ртути для утилизации можно узнать по номеру 112.
Как собрать ртуть с помощью магнита?
Это значит, что вопрос, как собрать ртуть магнитом, имеет единственно верный ответ — никак! Можно сколько угодно водить магнитом над ковром, диваном и другими местами розлива – от этого серебристые шарики не сдвинутся ни на миллиметр. Ртуть не магнитится!
Утилизация ртутьсодержащих отходов
Широкое применение ртути способствует высокой концентрации ее паров в атмосфере крупных городов. Сейчас повсюду используют люминесцентные лампы, которые содержат от 30 до 300 мг жидкого металла. А в некоторых лампах его в несколько раз больше. Согласно статистике, ежегодно около 100 млн. таких ламп становятся непригодными и требуют переработки. Лишь небольшая их часть проходит специальную утилизацию, а остальные сразу отправляются на свалку, где из-за разрушения целостности стекла ртуть попадает в атмосферу.
Кроме того, ртуть применяется в производстве аккумуляторов и батарей, которые в основном никак не перерабатываются. Таким путем за год на свалку попадает около 40 тонн ртути. Эта цифра очень большая, поэтому проблема утилизации ртутьсодержащих предметов стоит очень остро. Бесконтрольное обращение с ртутными отходами, безответственное отношение к приборам, содержащим этот жидкий металл, создает угрозу здоровью и жизни людей. Всем известно, какие неприятности может принести обычный градусник ртутный. Цена неумелого обращения с ним может стоить даже жизни.

Сейчас правительства всех стран работают над вопросом переработки ртутьсодержащих отходов. С этой целью создаются специальные компании, которые занимаются сбором непригодных к использованию приборов и ртутных предметов. Они разделяют их на компоненты (цоколи, стекло, металл) и перерабатывают. Из каждого вида отходов формируются блоки, которые упаковываются в специальную тару (чехлы, полиэтиленовые пакеты, канистры) и доставляются на место переработки.
- https://ru.wikipedia.org/wiki/%D0%A0%D1%82%D1%83%D1%82%D1%8C
- http://himsnab-spb.ru/article/ps/hg/
- http://www.kontren.narod.ru/x_el/info80.htm
- https://k-tree.ru/tools/chemistry/periodic.php?element=Hg
- http://ru.solverbook.com/spravochnik/ximiya/molyarnaya-massa/molyarnaya-massa-rtuti/
- https://remont.provocante-shoes.ru/kakoy/kakaya-valentnost-u-rtuti.html
- https://nauka.club/khimiya/rtut.html
- https://jgems.ru/metally/rtut
- https://uglevodorody.ru/publ/rtut-svoystva-dobycha-i-proizvodstvo-primenenie
- https://greenologia.ru/othody/metally/rtut
- https://FB.ru/article/174087/primenenie-rtuti-v-sovremennoy-promyishlennosti-svoystva-i-harakteristiki-rtuti
- https://bezotxodov.ru/rtut/primenenie-rtuti-v-sovremennoj-promyshlennosti
- https://atvmedia.ru/materials/chto-delat-esli-razbilsya-rtutnyy-gradusnik
- https://uchetovod.ru/mozhno-li-ubrat-rtut-magnitom
Ваша оценка?