Курс лекций по общей химии
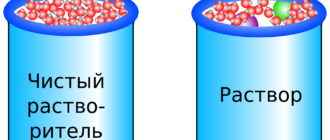
Над каждой жидкостью (растворителем или раствором) устанавливается определенное давление пара, насыщающего пространство. Это давление
Стехиометрия – раздел химии, рассматривающий количественные соотношения между реагирующими веществами. Закон сохранения массы: масса
1. Массовая доля – отношение (обычно процентное) массы растворенного вещества к массе раствора. Например,
Среди разнообразных химических реакций можно выделить два типа, существенно отличающихся друг от друга. К
В широком смысле растворы бывают газообразными, жидкими, твердыми. Примером газообразного раствора может
Способность химических элементов присоединять или отдавать электроны связана со строением атомов и положением их
Давление имеет существенное значение при реакциях между газами.В результате увеличения давления повышается концентрация реагирующих
Ранее рассматривались связи, обусловливающие образование молекул из атомов. Однако между молекулами также существует
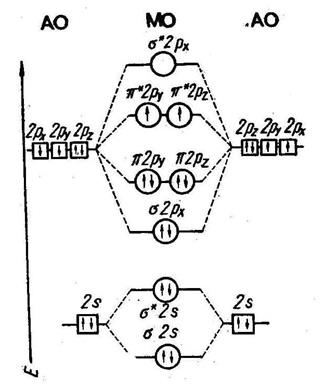
Существование связывающих и разрыхляющих МО подтверждается физическими свойствами молекул. Метод МО позволяет предвидеть,
Если раствор и растворитель разделены полупроницаемой (т.е. проницаемой только для растворителя) мембраной, то растворитель
Наряду с понижением давления пара изменяются также температуры кипения и замерзания указанных растворов. Растворы
МО для молекул с различными атомами (NO, CO) строятся аналогично, если исходные атомы
В электрическом поле ион или молекула деформируются, т.е. в них происходит относительное смещение
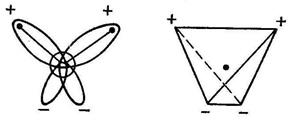
Важной характеристикой молекулы, состоящей более чем из двух атомов, является ее геометрическая конфигурация.
Установлено, что в ряде случаев определяющую роль в образовании химической связи играют не