Катализом называется изменение скорости химической реакции под действием веществ, химический состав и количество которых в результате реакции остаются неизменными. Эти вещества получили название катализаторов.
Скорость химической реакции в присутствии катализаторов может увеличиваться или уменьшаться. В первом случае говорят о положительном, во втором — об отрицательном катализе. Отрицательный катализ часто называют ингибированием, а вещества, вызвавшие его, — ингибиторами.
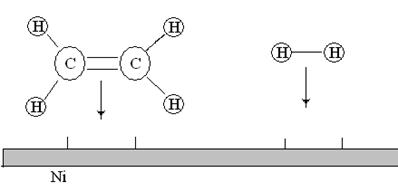
Различают гомогенный и гетерогенный катализ. При гомогенном катализе катализатор и реагирующие вещества образуют одну фазу. При гетерогенном катализе катализатор находится в системе в виде самостоятельной фазы, отделенной от других частей системы поверхностью раздела.
Пример гомогенного катализа: разложение растворенного в воде пероксида водорода присутствии находящихся в том же растворе иодид-ионов. Здесь реагирующие вещества и катализатор образуют однородную систему без границы раздела.
H2O2 + I- → IO- + H2O
H2O2 + IO- → H2O + O2 ↑ +I-
2H2O2 + I- → 2 H2O + I- +O2↑
Однако тот же диоксид серы, находясь в газообразном состоянии, способен окисляться кислородом воздуха на поверхности твердых катализаторов — оксидов ванадия, железа, хрома. В этом случае система будет гетерогенной и катализ — также гетерогенным.
Хотя во время реакции катализатор остается в химически неизменном состоянии и не расходуется, в некоторых случаях возможны его физические изменения. Это свидетельствуют о том, что катализатор на определенном этапе взаимодействует с реагентами, хотя в конечном итоге вновь выделяется — регенерируется.
Активные катализаторы снижают энергию активации процессов примерно на 25—40кДж/моль. Например, энергия активации разложения пероксида водорода составляет 75,4 кДж/моль, а в присутствии коллоидной платины падает до 49,0 кДж/моль. Поскольку в выражение константы скорости реакции энергия активации входит в отрицательный показатель:
k = A·e-Ea/RT
Даже незначительное уменьшение ее приводит к существенному возрастанию скорости реакции. Поэтому при 25 °С скорость каталитического разложения пероксида водорода больше скорости разложения в отсутствие катализатора примерно в 42600 раз.
Катализ широко используется в химической промышленности и в смежных с ней отраслях, так как это способствует резкому повышению производительности технологических процессов. Окисление сернистого ангидрида в серный при получении серной кислоты, конверсия углеводородного сырья до водорода и оксида углерода(II)—исходного компонента для получения аммиака и метанола, окисление аммиака при производстве азотной кислоты, получение жидкого моторного топлива на основе ископаемых углей, гидрогенизация растительных масел и др. — вот далеко не полный перечень примеров промышленного применения каталитических реакций.
Иногда оказывается желательным замедлить химические реакции, и тогда в системы вводят ингибиторы. Например, с помощью специально подобранных ингибиторов замедляют окислительные процессы в смазочных маслах, пищевых жирах, дизельном топливе, полимеризацию и старение полимеров.
Ваша оценка?