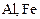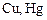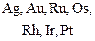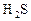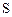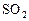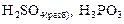
по схеме:
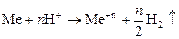 .
.
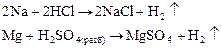
Окисление металлов за счет кислотного остатка происходит водными растворами тех кислот, центральный атом которых может понижать свою степень окисления, в результате чего анион этой кислоты может выступать в роли окислителя.
в качестве окислителя формально выступает азот в степени окисления +5. Данные приведены в табл. 4.
Таблица 4
|
|
||||
|
Активные |
Средней активности |
Малоактивные |
||
|
Реагируют |
Реагируют, реагируют и пассивируется: |
Реагируют: |
Не реагируют:
|
|
|
Кислота восстанавливается, в основном, до следующих продуктов |
||||
|
|
|
|
– |
|
Например:
Активные металлы реагируют следующим образом:
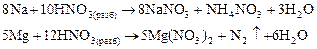
Металлы средней активности восстанавливают азот до N+1:
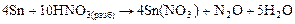
Малоактивные металлы реагируют с выделение NO или NO2:
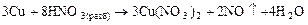
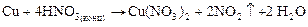
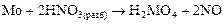
может происходить более глубокое восстановление N+5. Данные приведены в табл. 5.
Таблица 5
|
|
|||
|
Активные |
Средней активности |
Малоактивные |
|
|
Реагируют |
Реагируют, реагируют и пассивируются:
|
Реагируют: |
Не реагируют:
|
|
|
|
Например:
Активные металлы глубоко восстанавливающие азот:
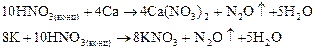
Металлы средней активности выделяют NO или NO2:
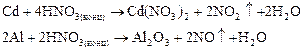
Малоактивные металлы восстанавливают азот до N+4:
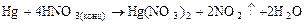
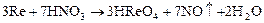
, а также некоторые малоактивные металлы. Данные приведены в табл. 6.
Таблица 6
|
|
|||
|
Активные |
Средней активности |
Малоактивные |
|
|
Реагируют |
Реагируют, реагируют и пассивируются: |
Реагируют: |
Не реагируют:
|
|
Кислота восстанавливается, в основном, до следующих продуктов |
|||
|
|
|
|
– |
Например:
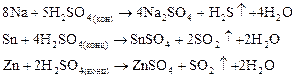
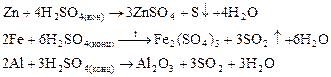
Малоактивные металлы восстанавливают серу до S+4:
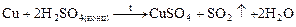
Ваша оценка?


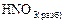 (окислитель
(окислитель 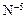 )
)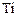
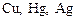
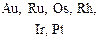
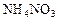
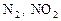
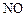
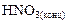 (окислитель
(окислитель 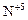 )
)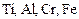
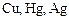
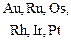
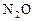
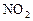
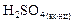 (окислитель
(окислитель 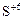 )
)