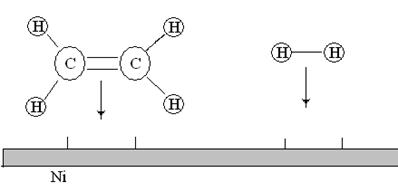
Рассмотрим экзотермическую реакцию:
СО + 2Н2=> СН3ОН — 93,5 кДж
Действие энтальпийного фактора обусловливает ее протекание в прямом направлении.
∆H <0 (процесс экзотермический)
Однако наибольшее значение энтропии достигается при полном разложении метанола на водород и оксид углерода, так как при этом число молекул газов возрастает втрое.
Вычислим изменение энтропии системы при прямой реакции.
Изменение энтропии в ходе химической реакции ( ΔS) равно сумме энтропий продуктов за вычетом суммы энтропии исходных веществ.
Таблица 3. Стандартные энтропии веществ-участников реакции
|
Вещество |
Стандартная энтропия, S0 Дж/моль·K |
|
CO (газ) |
197,5 |
|
H2(газ) |
130,5 |
|
CH3OH (газ) |
240,1 |
ΔS° = 240,1 Дж/моль·K· 1 моль —(197,5 Дж/моль·K· 1 моль + 130,5 Дж/моль·K· 2 моль) = -218,4 Дж/К.
Отсюда, при синтезе метанола энтропия уменьшается.
Таким образом энтальпийный и энропийный факторы действуют в противоположных направлениях.
Для того чтобы учесть действие обоих факторов в термодинамике используется функция состояния системы — энергия Гиббса (G). Она применяется для изобарно-изотермических условий и связана с энтальпией и энтропией простым соотношением:
G = H — TS.
Изменение энергии Гиббса в ходе химической реакции:
∆G = ∆H — T∆S
Характер этого изменения позволяет судить о принципиальной возможности или невозможности осуществления процесса.
При постоянных давлении и температуре самопроизвольно протекают только такие химические реакции, которые сопровождаются уменьшением энергии Гиббса.
Иными словами, ∆G < 0 (т.е. энергия Гиббса системы в исходном состоянии больше, чем в конечном) свидетельствует о возможности самопроизвольного осуществления реакции. Если же ∆G > 0, то процесс не может идти в данных условиях.
Используя известные значения стандартных энтальпий образования и стандартных энтропии веществ, можно прогнозировать возможность протекания химической реакции при той или иной температуре.
Под стандартной энергией Гиббса образования понимают изменение энергии Гиббса при реакции образования 1 моль данного соединения из простых веществ. Подобно энтальпии и энтропии:
стандартное изменение энергии Гиббса в ходе химической реакции равно сумме стандартных энергий Гиббса образования продуктов реакции за вычетом суммы стандартных энергий Гиббса образования исходных веществ.
Пользуясь табличными данными можно рассчитать изменение энергии Гиббса в стандартных условиях.
Рассмотрим обратимую реакцию:
N2 (г) +ЗН2 (г) ↔ 2NH3(г) .
Для стандартных условий ∆H° = — 92,4кДж ∆S°= -0,1978 кДж/К
Изменение энергии Гиббса:
∆G0 = ∆H0 — T∆S0 = -92,4 — (0,198 ∙ 298) = 92,4 + 59,0 = -33,4 кДж.
Итак, при стандартных условиях реакция протекает в прямом направлении, хотя она сопровождается уменьшением энтропии (превалирует энтальпийный фактор). Обратная реакция — разложение аммиака на водород и азот — в этих условиях термодинамически (принципиально) невозможна.
Однако по мере повышения температуры все более существенным становится влияние энтропийного фактора.
∆G500 = 6,6 кДж,
∆G800 = 66,0 кДж.
В случае обратной реакции ∆G имеют, естественно, противоположные знаки. Уже при 500К становится принципиально возможным разложение аммиака. При 800К эта возможность возрастает.
Когда действия энтальпийного и энтропийного факторов уравновешивают друг друга, т.е. ∆G=0, наступает состояние химического равновесия. В этом случае скорость прямой реакции равна скорости обратной.
Константа химического равновесия связана с изменением энергии Гиббса уравнением: ΔGреак. = -RT In К
Изменение энергии Гиббса определяет лишь возможность протекания химических реакций. В конкретных условиях скорость протекания реакции может быть бесконечно мала. Это обусловлено барьером энергии активации, при нагревании или освещении солнечным светом реакция немедленно произойдет.
Ваша оценка?