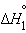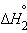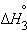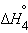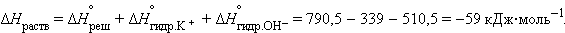Стандартная энтальпия образования  – тепловой эффект реакции образования одного моля вещества из простых веществ, его составляющих, находящихся в устойчивых стандартных состояниях.
– тепловой эффект реакции образования одного моля вещества из простых веществ, его составляющих, находящихся в устойчивых стандартных состояниях.
Например, для реакций
|
Реакция |
Энтальпия образования |
|
Na2O(т) + H2O(ж) = 2NaOH(т) |
|
|
1/2Na2O(т) + 1/2H2O(ж) = NaOH(т) |
|
|
Na(т) + 1/2O2(г) + 1/2H2(г) = NaOH(т) |
|
|
2Na(т) + O2(г) + H2(г)= 2NaOH(т) |
|
только 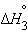 является стандартной энтальпией образования NaOH.
является стандартной энтальпией образования NaOH.
Энтальпия образования простых веществ принята равной нулю, причем нулевое значение энтальпии образования относится к агрегатному состоянию, устойчивому при T = 298 K. Так, для йода 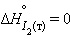 кДж∙
кДж∙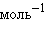 ,
, 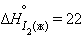 кДж∙
кДж∙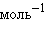 ,
, 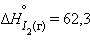 кДж∙
кДж∙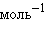 . Для углерода
. Для углерода 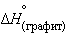 = 0 кДж∙
= 0 кДж∙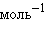 ,
, 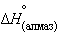 = 1,83 кДж∙
= 1,83 кДж∙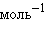 .
.
Стандартная энтальпия сгорания 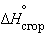 – тепловой эффект реакции сгорания одного моля вещества до образования высших оксидов. Для органических веществ – до
– тепловой эффект реакции сгорания одного моля вещества до образования высших оксидов. Для органических веществ – до 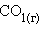 и
и 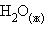 . Теплота сгорания негорючих веществ принимается равной нулю. Теплота сгорания топлива характеризует его теплотворную способность.
. Теплота сгорания негорючих веществ принимается равной нулю. Теплота сгорания топлива характеризует его теплотворную способность.
Энтальпия растворения складывается из теплоты разрушения кристаллической решетки (ΔHреш> 0) и теплоты гидратации (сольвататции для неводных растворов), выделяющейся в результате взаимодействия молекул растворителя с молекулами или ионами растворяемого вещества с образованием соединений переменного состава – гидратов (сольватов) (ΔHгидр < 0).
В зависимости от соотношения значений ΔHреш и ΔHгидр энтальпия растворения может иметь как положительное, так и отрицательное значение.
Так, энтальпия растворения КОН – отрицательная величина и характеризует экзотермический процесс:
|
|
|
|
Растворение же 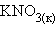 – эндотермический процесс (ΔH = 35,9 кДж∙
– эндотермический процесс (ΔH = 35,9 кДж∙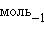 ), так как на разрушение кристаллической решетки (
), так как на разрушение кристаллической решетки (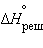 = 684,5 кДж∙
= 684,5 кДж∙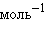 ) затрачивается больше энергии, чем выделяется при гидратации ионов
) затрачивается больше энергии, чем выделяется при гидратации ионов 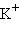 и
и  : –339 и –309,6 кДж∙моль–1 соответственно.
: –339 и –309,6 кДж∙моль–1 соответственно.
Стандартная энтальпия нейтрализации 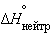 – энтальпия реакции взаимодействия сильных кислот и оснований с образованием одного моля
– энтальпия реакции взаимодействия сильных кислот и оснований с образованием одного моля 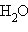 при стандартных условиях.
при стандартных условиях.
|
|
HCl + NaOH = NaCl + H2O; |
|
|
|
H+ + OH– = H2O, ΔH ° = –55,9 кДж∙моль–1. |
|
Для концентрированных растворов сильных электролитов 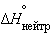 может быть различным из-за изменения значения
может быть различным из-за изменения значения 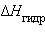 их ионов при разбавлении.
их ионов при разбавлении.
Стандартная энтальпия реакции ΔH ° – тепловой эффект реакции определенного числа молей реагентов, задаваемого уравнением реакции при стандартных условиях. Например, для реакции
|
|
4H2O(ж) + 2Fe(т) → Fe2O3(т) + 4H2(г), ΔH ° = 321,3 кДж |
|
ΔH ° относится целиком к реакции, как она записана.
Стандартная энтальпия разрыва связи 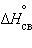 (называемая также энергией связи
(называемая также энергией связи 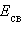 ) – энергия, поглощаемая при разрыве связей двух атомов одного моля вещества, находящегося в газообразном состоянии при 298 К:
) – энергия, поглощаемая при разрыве связей двух атомов одного моля вещества, находящегося в газообразном состоянии при 298 К:
|
|
HCl(г) → H(г) + Cl(г), ΔH ° = 429,7 кДж. |
|
Средние стандартные энтальпии связи могут быть определены для индивидуального соединения или путем усреднения значений, найденных для целых классов соединений.
Ваша оценка?