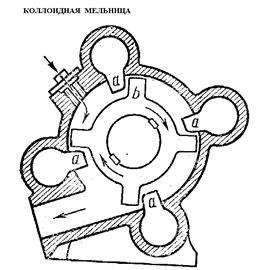
Гетерогенные дисперсные системы, в том числе и золи, могут быть получены: 1. Диспергированием, т.е.
Согласно современным представлениям, в центре атома находится ядро (nucleus). Оно имеет очень маленькие размеры,
Многие химические реакции протекают самопроизвольно, т.е. без затрат энергии извне. Одной из движущих сил
Мерой неупорядоченного состояния системы служит термодинамическая функция, получившая название энтропии. Состояние системы можно характеризовать
Различают три типа окислительно–восстановительных реакций: межмолекулярные, внутримолекулярные и реакции самоокисления–самовосстановления. A. Межмолекулярные – это
Благородные газы имеют электронную конфигурацию ns2np6 (у гелия 1s2) и составляют VIIIА группу. По
Коррозия — это самопроизвольный процесс разрушения металлов под влиянием внешней среды. Причиной коррозии является
К общим свойствам растворов относятся: понижение давления насыщенного пара растворителя над раствором, температура замерзания,
К элементам III группы главной подгруппы относятся: бор, алюминий, галлий, индий, таллий. В представленной
Химическая термодинамика — наука, изучающая переходы энергии из одной формы в другую при химических
Квантовое число n – главное. Оно определяет энергию электрона в атоме водорода и одноэлектронных
К числу сильных окислителей, широко используемых на практике, относятся галогены (Fe2, Cl2, Br2, I2),
Составление ионно-молекулярных уравнений Реакции в водных растворах электролитов являются реакциями между ионами. Они
— бескислородные кислоты получают взаимодействием водорода с неметаллами (с последующим растворением в воде):
Данный тип связи хар-н для соединений в которых Н связывается с каким либо электроотрицательным