На схеме показано образование молекулы водорода. Из двух 1s – орбиталей атомов водорода возникают две молекулярные орбитали. Одна из них сигма-связывающая σ1sсв , другая сигма-разрыхляющая σ1sразр . Связывающая орбиталь обладает меньшей энергией, чем исходные атомные орбитали, а разрыхляющая большей. Поэтому электроны переходят на связывающую орбиталь – см. рисунки 7 и 8.
2 H (1s1) → H2 [(σсв.1s)2] — 435 кДж
Уменьшение энергии при переходе электронов с атомных на молекулярные орбитали и делает возможным образование химической связи и, соответственно, молекулы водорода.
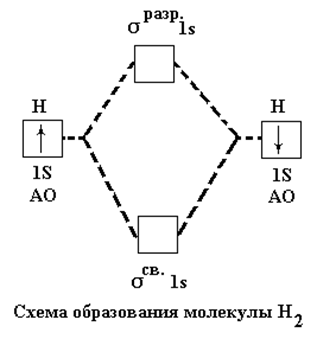
Рис.7 Образование молекулярных орбиталей в молекуле водорода
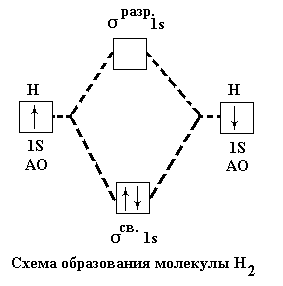
Рис.8. Образование связывающей орбитали в молекуле водорода
Метод МО позволяет объяснить факт существования иона H2+. При его образовании единственный электрон переходит с атомной орбитали 1 s на связывающую орбиталь σсв.1s, что энергетически выгодно и сопровождается выделением энергии:
H (1s1) + H+ → H2+ [(σсв.1s)1] + 259 кДж
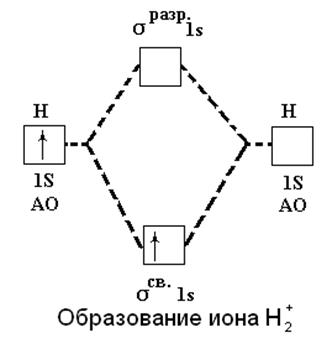
Рис.9. Образование иона водорода
Метод МО позволяет объяснить и то, почему не могут существовать некоторые частицы. Например, экспериментально обнаружен молекулярный ион He2+. Из трех электронов, входящих в его состав, два занимают связывающую (σ1sсв.)2 орбиталь, энергия которой меньше, чем у исходных 1s орбиталей, и один разрыхляющую σ1s разр, энергия которой больше исходных 1s орбиталей. В итоге энергия молекулярного иона гелия оказывается меньше, чем суммарная энергия исходных атома и иона гелия, что и определяет возможность его существования. Однако в молекуле гелия He2, если бы таковая существовала, число электронов на связывающей и разрыхляющей орбиталях было бы одинаково и равно двум. Поэтому энергетического выигрыша по сравнению с суммарной энергией двух атомов гелия быть не может, именно поэтому молекул гелия не существует.
Ваша оценка?