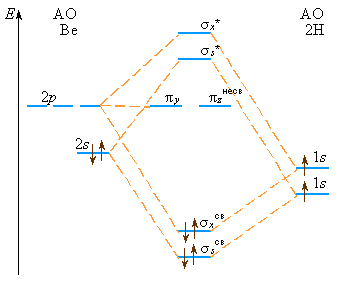
Рассмотрим некоторые многоатомные молекулы. Линейную молекулу BeH2 (существующую лишь в газовой фазе) образуют 1s-АО двух атомов водорода, одна 2s- и одна 2px-АО бериллия (рис 3.14). Им соответствуют две σ- и две σ*-МО. Но общее число участвующих в образовании МО BeH2 АО равно шести. Поэтому две из них не вносят вклад в стабилизацию молекулярной системы. Эти МО (πy,πz) называются несвязывающими.
|
|
|
Рисунок 3.14. Энергетическая диаграмма МО молекулы BeH2. |
Электронная конфигурация 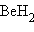 –
– 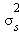
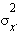 Поскольку четыре валентных электрона располагаются на связывающих орбиталях, кратность трехцентровой связи равна двум. Обе электронные пары в молекуле
Поскольку четыре валентных электрона располагаются на связывающих орбиталях, кратность трехцентровой связи равна двум. Обе электронные пары в молекуле 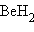 в равной степени принадлежат обоим атомам H, т. е. связи Be – H равноценны, поэтому каждой двухцентровой связи Be – H соответствует кратность 1.
в равной степени принадлежат обоим атомам H, т. е. связи Be – H равноценны, поэтому каждой двухцентровой связи Be – H соответствует кратность 1.
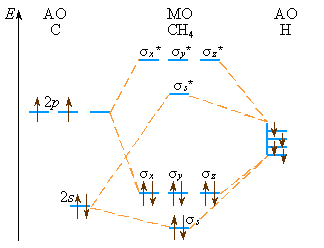
Аналогично составляются схемы МО и для других многоатомных молекул. В линейные комбинации включают только близкие по энергии и перекрывающиеся АО. Например, для тетраэдрической молекулы метана линейные комбинации из одной 2s-, трех 2px-, 2py-, 2pz-орбиталей углерода и четырех 1s-орбиталей водорода образуют σs, σs* и по три трехкратно вырожденных σsp связывающих и σsp* разрыхляющих MO, соответствующие четырем полностью равноценным пятицентровым связям. По характеру распределения электронной плотности все связи в молекуле CH4 равноценны. Существенно, что любой валентный электрон в молекуле CH4 может оказаться вблизи любого ее атома – связи в молекуле CH4 делокализованы (рис 3.15).
|
|
|
Рисунок 3.15. Энергетическая диаграмма образования МО молекулы CH4. |
Ваша оценка?