Пример 9. Определите молярную концентрацию вещества (моль/дм3) в растворе с массовой долей фосфорной кислоты 60,8 % (р = 1,43 г/см3).
Решение. М(Н3РО4) = 98 г/моль.
Вариант I
Массу вещества выражаем из формулы (4.1):
т(вещества) = w×m(pacmвopa).
Объем раствора равен:
V(раствора) = т(раствора)/р(раствора).
Значения массы вещества и объема раствора подставим в выражение (4.5):
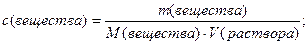
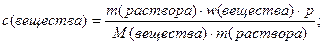
Масса раствора постоянна, она сокращается и мы получаем следующее выражение:
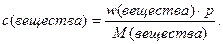
Подставляем значения:
c(H2SO4) = 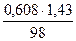 = 0,00887 моль/см3 = 8,87 моль/дм3. 98
= 0,00887 моль/см3 = 8,87 моль/дм3. 98
Вариант II
Найдем массу Н3РО4 в 1 дм3 раствора.
Масса 1 дм3 раствора:
т(раствора) = 1,43 г/см3×1000 см3= 1430 г.
В 100 г раствора содержится 60,8 г Н3РО4,
в 1430 г раствора содержится х г Н3РО4.
Откуда х=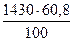 =869,4 г.
=869,4 г.
В 1 дм3 раствора содержится n(Н3РО4) =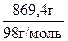 = 8,87 моль
= 8,87 моль
кислоты, значит, с = 8,87 моль/дм3.
Ответ: 8,87 моль/дм3.
Пример 10. Найти массовую долю вещества в растворе с концентрацией КОН 1,6 моль/дм3. Плотность раствора 1,075 г/см3.
Решение. Вариант I
В 1 дм3 раствора массой т(раствора) = 1,075×1000 = 1075 г содержится 1,6 моль или т(вещества) = 1,6×56 = 89,6 г КОН.
В 1075 г раствора содержится 89,6 г КОН,
в 100 г раствора — х г КОН.
Откуда х = 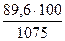 = 8,33. Значит, w(KOH) = 8,33 %.
= 8,33. Значит, w(KOH) = 8,33 %.
Вариант II
Если составить уравнение, выражающее массовую долю, то для 1 дм3 раствора получим:
w(КОН)=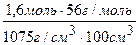 = 0,0833 = 8,33 %
= 0,0833 = 8,33 %
Ответ: 8,33 %.
Пример 11. Соотношение между молекулами метанола и воды в растворе составляет 1:4. Определите массовую, объемную доли и концентрацию СН3ОН (моль/дм3) в растворе, если плотности составляют: СН3ОН — 0,79 г/см3, Н2О — 1,0 г/см3 (считать объем смеси равным сумме объемов компонентов).
Решение. Соотношение между молекулами такое же, как между количествами веществ, т. е. на 1 моль спирта приходится 4 моль воды.
Пусть раствор содержит 1 моль СН3ОН и 4 моль Н2О (можно рассмотреть 4 моль СН3ОН и 16 моль Н2О и т. д.). Тогда
m(CH3OH)=1×32=32 г, m(H2O)=4×18=72 г,
а из выражения (4.1):
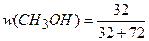 = 0,308.
= 0,308.
Объем СН3ОН, необходимый для приготовления раствора,
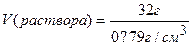 = 40,5 см3,
= 40,5 см3,
объем воды V(растворителя) = 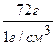 = 72 см3.
= 72 см3.
По условию, объем раствора равен сумме объемов компонентов, тогда из выражения (4.3):
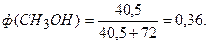
В 112,5 см3 раствора содержится 1 моль СН3ОН,
в 1000 см3 раствора — х моль СН3ОН.
… , ,
Откуда х =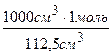 = 8,89 моль, т. е. с = 8,89 моль/дм .
= 8,89 моль, т. е. с = 8,89 моль/дм .
Ответ. w(CH3OH) = 30,8 %; ф(СН3ОН) = 36 %; с(СН3ОН) = 8,89 моль/дм3.
Ваша оценка?








