Алканы — что это такое в химии
Алканы — являются предельными углеводородами, которые содержат только одинарные связи между атомами С-С в молекуле, то есть содержат максимально возможное количество атомов водорода в молекуле.
Молекулы алканов характеризуются наличием следующих химических связей:
- С-Н;
- С-С.
Связь С-Н является ковалентной слабополярной, связь С-С — ковалентной неполярной. Данные связи относят к типу одинарных σ-связей. В алканах атомами углерода сформировано по четыре σ-связи. Таким образом, тип гибридизации атомов углерода в молекулах алканов — sp3:
Когда образуются связи С-С, перекрываются sp3-гибридные орбитали атомов углерода:
Процесс формирования связи С-Н сопровождается перекрыванием sp3-гибридной орбитали атома углерода и s-орбитали атома водорода:
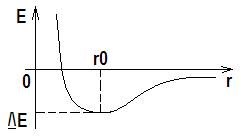
Четыре sp3-гибридные орбитали атома углерода отталкиваются друг от друга и занимают такое положение, при котором угол между орбиталями обладает максимальным значением. По этой причине четыре гибридные орбитали углерода в алканах расположены в пространстве под углом 109028′ относительно друг друга:
Данное строение молекулы называется тетраэдрическим. В качестве примера можно привести молекулу метана CH4. В ней расположение атомов водорода совпадает с вершинами тетраэдра, центр которого соответствует атому углерода.
В молекулах линейных алканов атомы углерода расположены зигзагообразно. К примеру, н-бутан характеризуется зигзагообразным пространственным строением.
Особенности этана
Данный парафин является вторым в гомологическом ряду алканов. Он имеет в сравнении с ним более высокую температуру кипения. Оба этих насыщенных углеводорода являются гомологами. Они имеют сходное химическое строение, подобные свойства. Единственным отличием между ними является группа СН2, которая называется гомологической разницей.
Рассмотрим еще один вариант того, как получить этан из метана. Например, можно осуществить частичное окисление метана до ацетилена. Полученный алкин, имеющий тройную связь в молекуле, подвергается каталитическому гидрированию. Продуктом взаимодействия будет именно этан. Осуществляется гидрирование по радикальному механизму. Несмотря на многообразие вариантов, для того чтобы определиться, как получить этан из метана, необходимо проанализировать условия протекания каждого отдельного процесса.
В настоящее время ответом на вопрос о том, как получить этан из метана, являетя частичное окисление с последующим гидрированием.

Строение
Параметры молекулы этана
Молекула этана имеет тетраэдрическое строение: атомы углерода являются sp3-гибридными. Связь C–C образована перекрыванием sp3-гибридных орбиталей, а связь C–H — перекрыванием sp3-гибридной орбитали углерода и s-орбитали водорода. Длина связи C–C равна 1,54 Å, а длина связи C–H равна 1,095 Å.
Поскольку С–С-связь в этане одинарная, вокруг неё возможно свободное вращение метильных групп. При вращении возникают различные пространственные формы молекулы этана, которые называются конформациями. Конформации принято изображать в виде перспективного изображения (такие изображения иногда называют «лесопильными козлами») либо в виде проекций Ньюмена.
Число конформаций для этана бесконечно, однако принято рассматривать две крайние конформации:
- заслонённую, в которой атомы водорода максимально сближены в пространстве;
- и заторможенную, в которой атомы водорода максимально удалены.
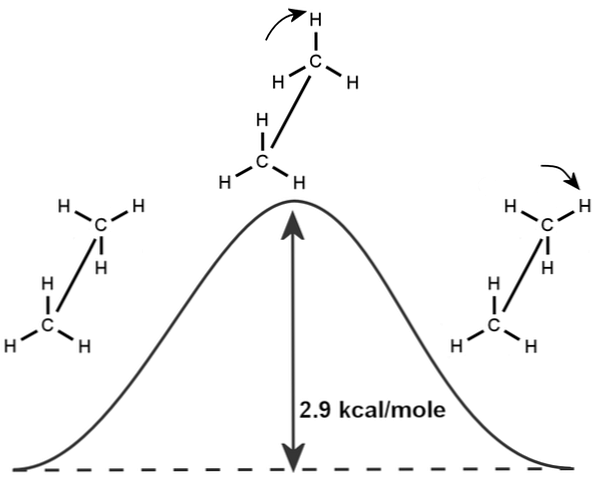
Заслонённая конформация имеет наибольшую энергию из всех конформаций, а заторможенная — наименьшую, то есть является наиболее энергетически выгодной и, следовательно, более устойчивой. Разница энергии между этими конформациями равна 2,9 ккал/моль. Считается, что это число отражает торсионное напряжение в менее выгодной заслонённой конформации. Если разделить эту энергию на три взаимодействия между парами атомов водорода, то энергия торсионного взаимодействия двух атомов водорода составит примерно 1 ккал/моль.
По значению 2,9 ккал/моль из уравнения Гиббса можно вычислить константу равновесия между двумя конформациями этана. При температуре 25 °С значительно преобладает заторможенная конформация: 99 % молекул этана находятся в этой конформации и лишь 1 % — в заслонённой.
Энергии крайних и промежуточных конформаций принято представлять в виде циклических графиков, где по оси абсцисс отложен торсионный угол, а по оси ординат — энергия.
Физические свойства
Этан при н. у. — бесцветный газ, без запаха и вкуса. Молярная масса — 30,07. Температура плавления −183,23 °C, температура кипения −88,63 °C. Плотность ρгаз.=0,001342 г/см³ или 1,342 кг/м³ (н. у.), ρжидк.=0,561 г/см³ (T=-100 °C). Давление паров при 0 °C — 2,379 МПа. Растворимость в воде — 4,7 мл в 100 мл (при 20 °C), в этаноле — 46 мл в 100 мл (при 0 °C), хорошо растворяется в углеводородах. Точка вспышки у этана равна –187,8 °C, температура самовоспламенения — 595 °C. Этан образует с воздухом взрывоопасные смеси при содержании 5–15 об. % (при 20 °C). Октановое число —120,3.
Химическая структура
Этан является молекулой с формулой С2H6, обычно рассматривается как объединение двух метильных групп (-CH3) с образованием углеводорода простой углерод-углеродной связи. Это также самое простое органическое соединение после метана, представленное следующим образом:
H3С-СН3
Атомы углерода в этой молекуле обладают sp-гибридизацией3, поэтому молекулярные связи имеют свободное вращение.
Также существует внутреннее явление этана, которое основано на одинаковом вращении молекулярной структуры и минимальной энергии, необходимой для вращения связи на 360 градусов, которое ученые назвали «этановым барьером»..
По этой причине этан может встречаться в различных конфигурациях в зависимости от его вращения, даже если существует более стабильная конформация, когда атомы водорода находятся напротив друг друга (как показано на рисунке)..
Синтез этана
Этан может быть легко синтезирован из электролиза Колбе, органической реакции, в которой происходят две стадии: электрохимическое декарбоксилирование (удаление карбоксильной группы и выделение углекислого газа) двух карбоновых кислот и комбинация продуктов промежуточные соединения с образованием ковалентной связи.
Точно так же электролиз уксусной кислоты приводит к образованию этана и углекислого газа, и эта реакция используется для синтеза первого.
Окисление уксусного ангидрида под действием пероксидов, концепция, аналогичная концепции электролиза Колбе, также приводит к образованию этана.
Таким же образом он может быть эффективно отделен от природного газа и метана процессом сжижения с использованием криогенных систем для улавливания этого газа и отделения его от смесей с другими газами..
Для этой роли предпочтителен процесс турбонаддува: газовая смесь пропускается через турбину, создавая ее расширение, пока ее температура не опустится ниже -100ºC..
Уже на этом этапе компоненты смеси могут быть дифференцированы, так что жидкий этан будет отделен от газообразного метана и других видов, связанных с использованием перегонки.
Свойства
Этан встречается в природе как газ без цвета и запаха при стандартных давлениях и температурах (1 атм и 25 ° C). Он имеет температуру кипения -88,5 ºC и температуру плавления -182,8 ºC. Кроме того, он не подвержен воздействию сильных кислот или оснований..
Молекулы этана имеют симметричную конфигурацию и имеют слабые силы притяжения, которые удерживают их вместе, называемые силами рассеивания.
Когда пытаются растворить этан в воде, силы притяжения, возникающие между газом и жидкостью, очень слабы, поэтому очень трудно соединить этан с молекулами воды..
По этой причине растворимость этана является значительно низкой, слегка увеличиваясь при повышении давления в системе..
Этан может затвердеть, что приводит к образованию нестабильных кристаллов этана с кубической кристаллической структурой.
При понижении температуры выше -183,2 ° С эта структура становится моноклинной, что повышает стабильность ее молекулы.
Этот углеводород, даже если он широко не используется в качестве топлива, может использоваться в процессах сжигания для производства углекислого газа, воды и тепла, который представлен следующим образом:
2С2H6 + 7O2 → 4CO2 + 6H2O + 3120 кДж
Существует также возможность сжигания этой молекулы без избытка кислорода, который известен как «неполное сгорание» и который приводит к образованию аморфного углерода и оксида углерода в нежелательной реакции, в зависимости от количества применяемого кислорода. :
2С2H6 + 3О2 → 4C + 6H2O + Тепло
2С2H6 + 4О2 → 2C + 2CO + 6H2O + Тепло
2С2H6 + 5О2 → 4CO + 6H2O + Тепло
В этой области сгорание происходит посредством ряда свободнорадикальных реакций, которые пронумерованы сотнями различных реакций. Например, такие соединения, как формальдегид, ацетальдегид, метан, метанол и этанол, могут образовываться в неполных реакциях сгорания..
Это будет зависеть от условий, при которых протекает реакция, и от участия свободнорадикальных реакций. Этилен также может образовываться при высоких температурах (600-900 ºC), что является продуктом, весьма востребованным промышленностью..
Окислительное дегидрирование этана
Реакция окислительного дегидрирования этана (ОДЭ) производится по следующей формуле:
C2H6 + 1/2O2 = C2H4 + H2O (1)
В качестве окислителя может применяться как концентрированный кислород, так и кислород в составе воздуха. Последние опыты по окислительному дегидрированию этана показали следующие результаты (в качестве окислителя применялся кислород с концентрацией 99,5 %):
- конверсия этана 74,0 %;
- селективность по этилену 82,0 %.
С использованием полученных данных была разработана схема выделения этилена из контактного газа окислительного дегидрирования этана, основанная на абсорбционном методе извлечении этан-этиленовой фракции. Принципиальная схема получения этилена путем ОДЭ представлена на рис. 2.
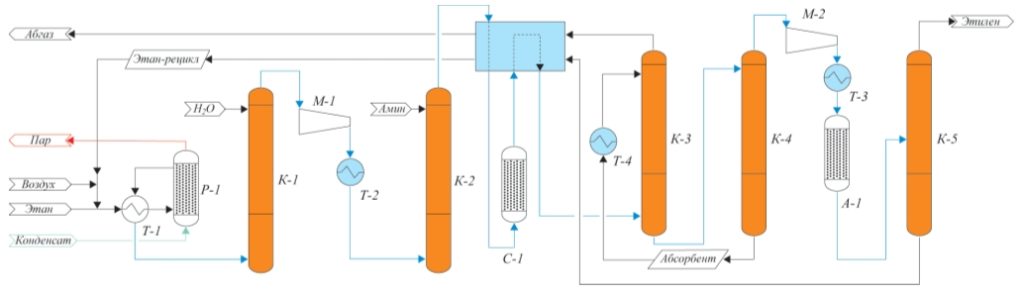
Рис. 2. Технология получения этилена методом ОДЭ
Схема включает реакционный узел Р-1, узел водной отмывки К-1, стадию предварительного удаления СО2 путем аминовой хемосорбции К-2, компримирования М-1, осушку С-1, колонны абсорбции и десорбции ЭЭФ (соответственно К-3 и К-4), колонну выделения товарного этилена К-5.
Разработанная технология является достаточно гибкой, чтобы проводить окислительное дегидрирование как концентрированным кислородом, так и кислородом воздуха или какой-либо промежуточной смесью воздухкислород. Для любого случая в зависимости от применяемого окислителя в представленной технологии решена проблема образования взрывоопасных смесей кислород-углеводороды-монооксид углерода, что делает технологию простой и безопасной.
Кроме того, гибкость технологии позволяет использовать различные катализаторы окислительного дегидрирования этана, т.е. при появлении новых катализаторов, являющихся по тем или иным характеристикам лучше ныне существующих, их также можно применять в данной технологической схеме.
Благодаря разработанной технологии, а также применению абсорбционной технологии выделения ЭЭФ из контактного газа, исключающей использование хладагентов с температурой ниже минус 37 °С, удалось достичь приемлемых для промышленной установки показателей эксплуатационных параметров. При моделировании технологии были получены следующие результаты:
Расходный коэффициент по сырью, т этана/т этилена 1,29
Расход электроэнергии, МВт⋅ч/т этилена 0,60
Степень извлечения этилена, % 98,5
Моделирование технологии ОДЭ с применением концентрированного кислорода показало значительно более низкие эксплуатационные затраты по сравнению с пиролизом этана (в качестве примера: потребление электроэнергии составляет соответственно 0,6 и 1,0).
Кроме того, технология ОДЭ имеет значительно более простую схему выделения этилена: отсутствуют узлы каталитического удаления ацетилена, низкотемпературного (до минус 100 °С) удаления метана и водорода и другие. В связи с этим данный способ получения этилена претендует на получение высоких результатов при дальнейших более подробных оценках экономической целесообразности реализации данного проекта.
Применение
Основное использование этана в промышленности — получение этилена методом парового крекинга. Именно из этилена далее получают важные промышленные продукты, однако в целях экономии разрабатываются методы превращения в них самого этана. Однако ни один из проектов пока не прошёл пилотную стадию. Проблемы в этой области связаны с низкой селективностью реакций. Одним из перспективных направлений является синтез винилхлорида напрямую из этана. Также применяется превращение этана в уксусную кислоту. Термическим хлорированием этана в различных условиях получают хлорэтан, 1,1-дихлорэтан и 1,1,1-трихлорэтан.
Физиологическое действие
Этан обладает слабым наркотическим действием (ослаблено за счёт низкой растворимости в жидкостях организма). Класс опасности — четвёртый. В концентрациях 2-5 об. % он вызывает одышку, в умеренных концентрациях — головные боли, сонливость, головокружение, повышенное слюноотделение, рвоту и потерю сознания из-за недостатка кислорода. В высоких концентрациях этан может вызвать сердечную аритмию, остановку сердца и остановку дыхания. При постоянном контакте может возникнуть дерматит. Сообщается, что при 15-19 об. % этан вызывает повышение чувствительности миокарда к катехоламинам.
- https://wika.tutoronline.ru/himiya/class/10/gomologicheskij-ryad-alkanov—poluchenie-i-primenenie
- https://www.syl.ru/article/289483/new_kak-poluchit-etan-iz-metana-uravnenie-opisanie-osobennosti-protekaniya
- https://visacon.ru/stati/24945-etan.html
- https://ru.thpanorama.com/articles/qumica/etano-estructura-propiedades-usos-y-riesgos.html
- https://chemtech.ru/alternativnye-metody-poluchenija-jetilena/
Ваша оценка?