Качественный анализ. Количественный анализ Химический анализ. Физико-химический анализ.
Идентификация — определение состава и строения неизвестного соединения путём сопоставления результатов анализа, а также физических и химических свойств этого соединения с соответствующими характеристиками известного.
По тождественности всех показателей устанавливают идентичность исследуемого неизвестного соединения известному.
Аналитическая реакция
Химическая реакция, сопровождающаяся аналитическим сигналом (признаком), по которому можно судить о наличии определяемого вещества, называется аналитической реакцией.
Аналитический сигнал (признак) – визуально наблюдаемое, инструментально фик-сируемое изменение свойств веществ (фазовое состояние, оптические и электрохимические параметры и т. д.).
К аналитическим сигналам (признакам) относят:
1. Образование (или растворение) осадка с определенными свойствами – цветом, растворимостью в определенных растворителях, формой кристаллов.
Пример: образование белого творожистого осадка хлорида серебра
AgNO3 + HCl → AgCl↓ + HNO3
3. Получение при действии реактива окрашенного растворимого соединения.
Пример: образование синего аммиаката меди
CuCl2 + 4NH3 → [Cu(NH3)4]Cl 2
Классификация аналитических реакций
1.Общие реакции – реакции, аналитические сигналы которых одинаковы для многих ионов.
2. Групповые реакции – частный случай общих реакций, используемых в конкретных условиях для выделения определенной группы ионов, обладающих близкими свойствами.
3. Селективными, или избирательными называют реакции, позволяющие в смеси ионов обнаруживать ограниченное число катионов или анионов.
4. Специфическими называют аналитические реакции, аналитический эффект которых характерен только для одного иона в присутствии других ионов.
Порядок химической идентификации сложных веществ
1. Отбор пробы для анализа. Средний состав пробы должен соответствовать среднему составу всей партии анализируемого объекта.
2. Разложение пробы и переведение ее в раствор. Пробу растворяют в воде или обрабатывают кислотами, при необходимости анализируемый материал сплавляют с различными веществами.
3. Проведение химической реакции. На определяемый компонент пробы Х воздействуют реагентом R, образуется продукт P:
Х + R → Р.
(аналитическая реакция).
4. Измерение какого-либо физического параметра (аналитического сигнала) продукта реакции, реагента или самого определяемого вещества.
Качественный анализ
Задачей качественного анализа является обнаружение отдельных элементов или ионов, входящих в состав смеси.
Эта задача может быть решена с помощью химических, физико-химических и физических методов анализа.
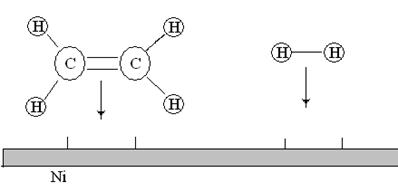
Пример: мокрый химический анализ
Разделение катионов на аналитические группы
Порядок выделения групп катионов
1. Пятая группа
Выделяется под действием соляной кислоты (групповой реагент), в результате чего образуются нерастворимые в кислотах осадки хлоридов серебра, свинца и ртути (I).
2. Четвертая группа
Выделяется под действием сероводорода (групповой реагент), в результате чего в осадок выпадают сульфиды меди, кадмия, висмута, ртути (II), сурьмы (III, V) и мышьяка (III, V), которые не растворяются в минеральных кислотах, но хорошо растворимы в HNO3 (кроме НgS).
3. Третья группа
Выделяется под действием раствора сульфида аммония (групповой реагент) в присутствии аммонийной буферной смеси (pH 9). При этом образуются малорастворимые гидроксиды алюминия и хрома, а также сульфиды железа (II, III), кобальта, никеля, марганца и цинка, растворимые в разбавленных минеральных кислотах.
4. Вторая группа
Осаждается под действием раствора карбоната аммония (групповой реагент) при pH около 9. В осадок выпадают карбонаты катионов второй аналитической группы – кальция, стронция и бария, хорошо растворимые в кислотах, в том числе и уксусной.
5. Первая группа
После отделения карбонатов второй группы в растворе остаются катионы аммония, натрия калия и магния, относящиеся к первой аналитической группе и не имеющие группового реагента.
Определение катионов в составе каждой группы проводится с использованием реагентов специфических для отдельных катионов.
Количественный анализ
Количественный анализ позволяет определить концентрацию (массу или количество) идентифицируемого вещества в пробе.
Используются химические и инструментальные (физические и физико-химические) методы.
Методы количественного анализа
1. Гравиметрические
2. Титриметрические
3. Оптические
4. Электрохимические
Гравиметрические методы анализа
Определяемый компонент выделяют из раствора в виде труднорастворимого соединения (метод осаждения) или летучего соединения (метод отгонки). Затем осаждаемую форму переводят в гравиметрическую форму, массу которой определяют взвешиванием.
Например, при количественном определении ионов Ca2+, осаждаемой формой является оксалат кальция CaC2O4, а гравиметрической CaO.
При определении в образце кристаллизационной воды методом отгонки, его навеску высушивают и прокаливают. О массе кристаллизационной воды можно судить по уменьшению массы образца или увеличению массы поглотителя водяных паров.
Методы гравиметрии обладают высокой точностью, но трудоемки и длительны, поэтому заменяются методами титриметрии и др.
Титриметрические методы анализа
Титрование осуществляется путем проведения реакций между определенным объемом стандартного раствора (раствора точно известной
концентрации), с раствором содержащим неизвестное количество определяемого вещества.
Стандартный раствор называется титрантом. Объем титранта, затрачиваемый на титрование, измеряют с помощью бюретки. Если объем и концентрация титранта известны, можно рассчитать количество определяемого (титруемого) вещества.
Оптические методы анализа
Спектрофотометрия – метод, основанный на избирательном поглощении раствором электромагнитного излучения в ультрафиолетовой, видимой или инфракрасной областях спектра.
Тест-системы
Тест-системы представляют собой простые, портативные, легкие и дешевые аналитические средства и соответствующие экспресс- методики для обнаружения и оценки концентрации веществ без существенной пробоподготовки и вне лаборатории.
При этом используются аналитические реакции, обеспечивающие получение визуально наблюдаемого и легко измеряемого аналитического сигнала (окрашивание бумаги или длина окрашенной части индикаторной трубки).
Сфера использования тест-систем
1. Экспресс-контроль технологических процессов;
2. Обнаружение метана в угольных шахтах;
3. Определение монооксида углерода и углеводородов в выхлопных газах автомобилей;
4.Обнаружение паров алкоголя в воздухе, выдыхаемом водителями и т.п.
Например, алкотест основан на изменении окраски, наступающей при реакции хромового ангидрида с парами, содержащими этанол.
3C2H5OH + 4CrO3 + 6H2SO4 → 3CH3COOH+ 2Cr2(SO4)3 + 9H2O
Физические методы исследования
Физический анализ. Новые методы химической идентификации и перспективы их внедрения.
Спектроскопические методы исследования
Основаны на изучении взаимодействия вещества с электромагнитным излучением.
Различают:
1.Спектры излучения (испускания);
2.Спектры поглощения (абсорбционные спектры);
3.Спектры рассеяния.
По используемым длинам волн различают спектроскопии
1. Инфракрасная (ИК) Длины волн: 700-105 нм
2. Видимая Длины волн: 400-700 нм
3. Ультрафиолетовая (УФ) Длины волн: 10-400 нм
Спектры испускания
В 1666 г. Исаак Ньютон разложил солнечный свет с помощью призмы в спектр и сделал вывод, что белый свет состоит из лучей разного цвета с различными показателями преломления.
Немецкие химики Густав Кирхгоф и Роберт Бунзен (60-е годы 19 века). Разработали методы получения спектров испускания нагретых в пламени горелки веществ и их использования для обнаружения химических элементов
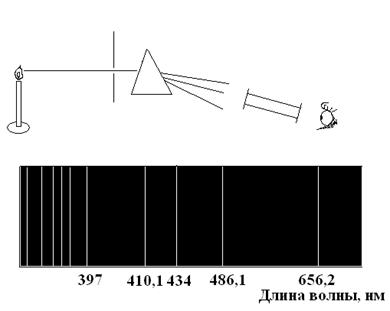
Рис. 26. Спектроскоп и спектр испускания водорода
Спектры испускания
Содержат набор полос, соответствующих частотам излучения, испускаемого веществом, находящимся в возбужденном состоянии. Состояние возбуждения достигается воздействием нагревания, света (фотовозбуждение), электрического разряда или химической реакции.
Спектры поглощения
Содержат набор полос, соответствующий частотам электромагнитных волн, которые поглощаются веществом.
В атомно-абсорбционном анализе вещество разогревают в графитовой трубке до 1500-20000 С электрическим током. Свет пропускают через застекленные торцы трубки и разлагают в спектр.
Спектры испускания и поглощения взаимнообратны
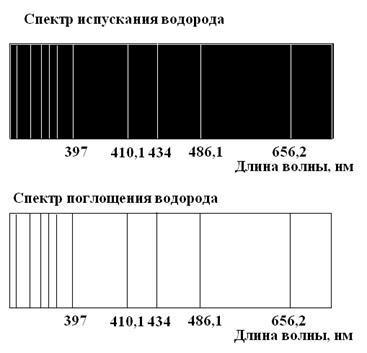
Рис. 27. Взаимная обратимость спектр испускания и поглощения водорода
Спектры комбинационного рассеяния
В процессе рассеяния может меняться длина волны света. Это явление носит название комбинационного рассеяния. Открыто в 1928 г. индийским физиком Ч. Раманом, Л.И. Мандельштамом и Г.С. Ландсбергом, поэтому называется рамановским рассеянием.
При этом в спектре монохроматического (лазерного) луча, прошедшего через жидкость, рядом с основной линией появляются дополнительные т.н. «стоксовы» и «антистоксовы» линии.
Механизм комбинационного рассеяния
Комбинационное рассеяние возникает вследствии колебаний дипольных молекул, индуцированных переменным электрическим полем волны света.
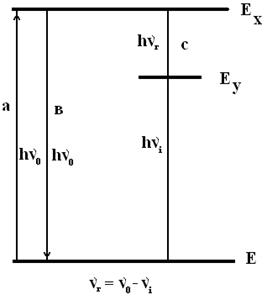
Рис. 28. Возникновение спектров комбинационного рассеяния (КР)
Анализ спектров КР позволяет выяснять строение молекул.
Пример: в спектре фосфористой кислоты (Н3РО3) была найдена частота, отвечающая валентному колебанию Р-Н
Инфракрасная спектроскопия
Энергия кванта ИК-излучения от 60 до 8 кДж/моль сответствует диапазону энергий колебаний ядер в молекулах и кристаллах и энергий теплового движения молекул и потому ИК излучение поглощается и его энергия переходит в энергию колебаний.
Характерные волновые числа колебаний групп атомов
1.≡С-H 3300-3340 см-1
2.=СH2 3080-3100 см-1
3. C6H5 -H 3000-3100 см-1
(Волновое число – величина, которая обратна длине волны).
Наличие характерных частот в (ИК) спектре поглощения позволяет обнаружить присутствие определенных групп атомов.
Интенсивность полос поглощения пропорциональна концентрации содержащих эти группы веществ.
Ультрафиолетовая и видимая спектроскопия
Энергия кванта УФ- и видимого излучения от 630 до 160 кДж/моль сответствует диапазону энергий перехода валентных электронов из основного состояния в возбужденное. Поглощение видимого излучения приводит к возникновению цвета вещества.
УФ и видимая спектроскопия позволяет делать выводы о строении соединений, характере химических связей, качественном и количественном составе.
Спектрофотометрия
Спектрофотометрия изучает связь спектров поглощения газообразных, жидких и твердых веществ с их составом и строением, а также с концентрацией их в растворах
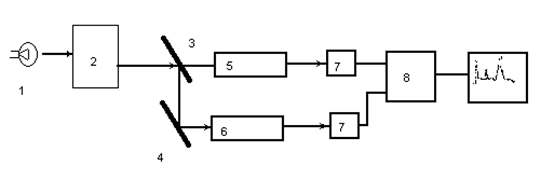
Рис. 29. Схема спектрофотометра
1. Источник света; 2. Монохроматор; 3. Полупрозрачное зеркало; 4. Зеркало; 5. Кювета с образцом; 6. Кювета сравнения; 7. Фотоприемник; 8. Усилитель.
Радиочастотная спектроскопия
Ядерный магнитный резонанс
Под действием поглощаемого излучения радиочастотного диапазона ядра в постоянном магнитном поле переходят из одного энергетического состояния (со спином антипараллельным полю) в другое (с параллельным полю спином).
Если непрерывно облучать образец слабым радиочастотным излучением (сотни мегагерц), а напряженность магнитного поля плавно менять с помощью электромагнита: последовательно создаются резонансные условия для различных ядер и избирательно поглощаются определенные частоты радиоизлучения.
Использование ЯМР-спектров
Спектр сравнивается со спектром известного вещества – делается вывод о наличии функциональных групп, содержащих ядра определенных элементов (часто водорода). Ядра водорода поглощают излучение различных частот в зависимости от химического окружения.
ЯМР как метод неразрушающего контроля
Если величина индукции магнитного поля меняется вдоль пространственных координат по определенному закону, то резонансная частота ЯМР окажется функцией не только вида ядер, но и координат точки.
Основанный на этом принципе метод послойного исследования тканей организма называется томографией («томос» — слой).
Ваша оценка?