Каждый атом гелия имеет на 1s-орбитали по два электрона, поэтому при образовании молекулярных орбиталей и связывающая, и разрыхляющая орбитали принимают по паре электронов (рис. 34).
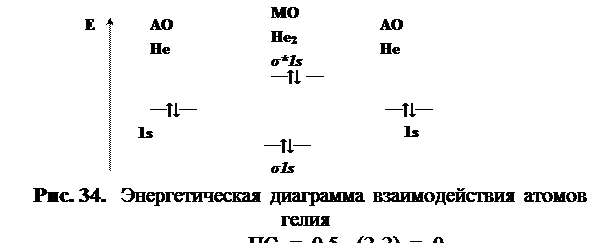 |
Квантово-механические расчёты показывают, что при заселении электронов на связывающую орбиталь выделяется меньше энергии, чем затрачивается при их переходе на разрыхляющую. Говорят, что разрыхляющая орбиталь разрыхляет сильнее, чем связывающая связывает. Поэтому для гелия энергетически более выгодно существовать в виде атомов, чем в форме молекул. Однако установлено существование молекулярного иона Не2+. Он образуется при взаимодействии атома гелия с катионом Не+. В этом случае на двух МО находится три электрона, два из которых занимают связывающую, а один — разрыхляющую МО (рис.35). Электронная формула катиона Нe2+ [(σ1s)2 (σ*1s)1].
 |
Ваша оценка?