4.Соли, образованные слабым основанием и слабой кислотой, подвергаются гидролизу и по катиону, и по аниону. Реакция растворов этих солей может быть нейтральной, слабокислой или слабощелочной в зависимости от значений константы диссоциации слабого основания и слабой кислоты, которые образуются в результате гидролиза.
Если Kд(осн) > Kд(кисл), то среда будет слабощелочной.
Если Kд(кисл) > Kд(осн), то среда будет слабокислой.
Если Kд(осн) = Kд(кисл), ионы соли гидролизуются в равной степени, и среда будет нейтральной.
Образующиеся в процессе гидролиза ионы 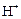 и
и 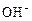 связываются в молекулы воды H2O, что приводит к смещению равновесия вправо, то есть к усилению гидролиза.
связываются в молекулы воды H2O, что приводит к смещению равновесия вправо, то есть к усилению гидролиза.
а) Соли, образованные однозарядными ионами:
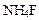 →←
→←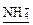 +
+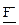
Записываются ионные уравнения по катиону и по аниону. Катион и анион объединяются в молекулу соли, а ионы 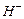 и
и 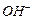 ‑ в молекулу воды:
‑ в молекулу воды:
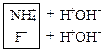 EQ \o(\s\up 3(→←
EQ \o(\s\up 3(→←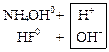
Для написания молекулярного уравнения надо сложить ионные уравнения, сократив лишние молекулы воды:
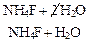 EQ \o(\s\up 3(→←
EQ \o(\s\up 3(→←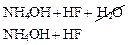
Kд(HF) > Kд(NH4OH), среда в растворе слабокислая, рН < 7.
б) Соли, образованные многозарядными ионами:
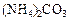 →←
→←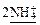 +
+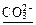
Записываются ионные уравнения по катиону и по аниону. Катион и анион объединяются в молекулу соли, а ионы 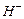 и
и 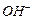 ‑ в молекулу воды. Остальные ионы дополняются противоионами, которые образуются при диссоциации соли
‑ в молекулу воды. Остальные ионы дополняются противоионами, которые образуются при диссоциации соли
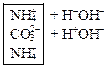 EQ \o(\s\up 3(→←
EQ \o(\s\up 3(→←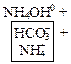
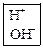
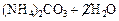 →←
→←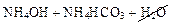
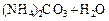 →←
→←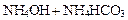
Kд(NH4OH) > Kд(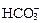 ), среда слабощелочная, рН > 7.
), среда слабощелочная, рН > 7.
Ваша оценка?





