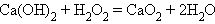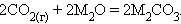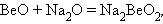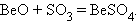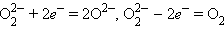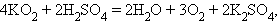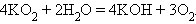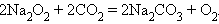При сжигании в атмосфере кислорода щелочных металлов образуются пероксиды M2O2. Только литий при обычных условиях сгорает в кислороде до Li2O. Начиная с калия, наряду с M2O2, образуются надпероксиды (KO2, RbO2, CsO2) и озониды (KO3, CsO3).
Щелочноземельные элементы при взаимодействии с кислородом при аналогичных условиях дают оксиды, пероксиды получаются труднее, чем для щелочных элементов. Так, пероксид бария BaO2 получают нагреванием на воздухе оксида бария при 700ºC. Пероксиды остальных металлов этой группы получают «мокрым» способом при действии пероксида водорода на гидроксиды:
|
|
|
|
Оксиды s-элементов имеют основной характер, что подтверждается характером их взаимодействия с кислотными оксидами:
|
|
|
|
Исключение, как и следует ожидать, составляет BeO – он амфотерен:
|
|
|
|
|
|
|
|
Пероксиды проявляют окислительно-восстановительную двойственность за счет пероксид-иона 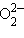 :
:
|
|
|
|
Окислительные свойства пероксидов выражены сильнее, чем восстановительные. Пероксиды и надпероксиды, как сильные окислители, легко разлагаются разбавленными кислотами и водой:
|
|
|
|
|
|
|
|
|
|
|
|
Последняя реакция используется для получения кислорода в подводных лодках и космических кораблях.
Гидроксиды s-элементов получают при взаимодействии оксидов с водой. Большой ионный радиус s-элементов (табл. 8.1) делает их гидроксиды сильными основаниями, а увеличение радиуса в группе сверху вниз приводит к усилению основности гидроксидов от Li к Cs и от Mg к Ba; амфотерен только Be(OH)2.
Ваша оценка?