Существует неполярная. В этом случае электроотрицательное взаимодействие атомов одинаковое (О2Н2).
Полярная – электроотрицательность атомов различна, но это отличие меньше чем в случае ионной связи.
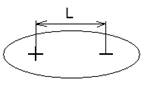 Чтобы оха-ть полярность, используют величину: дипольный момент: μ = q * l; q – заряд; l – расстояние.
Чтобы оха-ть полярность, используют величину: дипольный момент: μ = q * l; q – заряд; l – расстояние.
В отличии от ионной связи причиной образования ковалентной связи являются общие электронные пары.
Ковалентная связь является направленной, т.к. она образуется за счет перекрывания электронных облаков, а они имеют выраженное направление в пространстве.
Соединения с ковалентной связью могут образовывать молекулярные кристаллические решетки. В этом случае темпер. плавления и кипения очень низкая. Возможны и процессы сублимации.
Если же ковалентная связь осуществляется в атомной кристаллической решетке, то t плавления достаточно велика.
Ваша оценка?