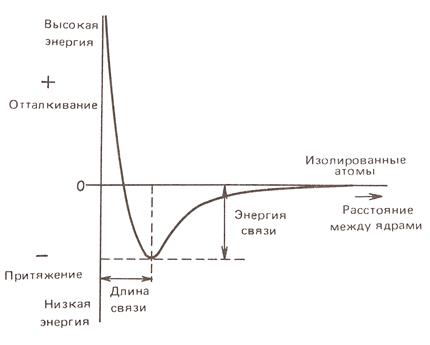
Перекрывание двух одноэлектронных атомных орбиталей — не единственный путь возникновения ковалентной связи. Атомы азота, кислорода, галогенов и некоторых других элементов в своих ковалентных соединениях имеют завершённые октеты, хотя не все орбитали их внешнего квантового слоя участвуют в образовании связей. Эти орбитали содержат n-электроны (nonbonding — не связывающие электроны) или неподелённые электронные пары (НЭП):
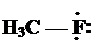 | |||||
|
Парами несвязывающих электронов при написании структурных формул обычно пренебрегают, однако их необходимо иметь в виду, т.к. они играют важную роль в проявлении химических свойств соединений. В частности, НЭП ответственны за способность веществ вступать во взаимодействие, при котором ковалентная связь образуется за счёт неподелённой электронной пары только одного партнёра (донора электронов), другой же атом (акцептор электронов) должен предоставить вакантную орбиталь. Это равносильно потере одного электрона донором и приобретению его акцептором, поэтому атомы, являющиеся партнёрами в образовании этой связи, меняют свои заряды.
Образованная таким путём ковалентная связь называется донорно-акцепторной, координационной или координативной. Существует четыре типа взаимодействия частиц, приводящих к образованию донорно-акцепторной связи.
1. Связь возникает при взаимодействии свободной орбитали катиона и НЭП аниона. Взаимодействуя друг с другом, обе частицы утрачивают заряды и образуют нейтральную молекулу.
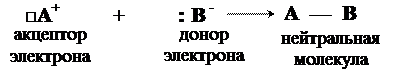 |
Примеры:
а) взаимодействие гидроксид-иона и катиона водорода (протона):
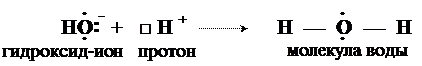 |
 б) взаимодействие бромид-аниона и метильного карбокатиона (карбокатионами называются органические катионы, имеющие положительный заряд на атоме углерода; carbon — углерод)
б) взаимодействие бромид-аниона и метильного карбокатиона (карбокатионами называются органические катионы, имеющие положительный заряд на атоме углерода; carbon — углерод)
в) взаимодействие метильного карбокатиона и метильного карбаниона
 |
2. Связь образуется при взаимодействии катиона (акцептор электронов) и нейтральной молекулы, имеющей во внешнем квантовом слое атомную орбиталь, несущую НЭП (донор электронов). Получается катион, у которого положительный заряд формально принадлежит атому-донору (фактически он распределяется по всей частице):

Оба взаимодействующих атома поменяли заряды: атом В, передав электрон катиону, зарядился положительно, катион А+, получив электрон, нейтрализовал свой заряд. Суммы зарядов в левой и правой частях уравнения одинаковы.
Формулы Льюиса позволяют подсчитать заряды на атомах, образующих донорно-акцепторные связи. Для этого предложена эмпирическая формула:
Z = G – N – B,
где Z — заряд атома, G — номер группы (число валентных электронов), N — число электронов НЭП, В — число двухэлектронных связей.
В качестве примеров можно привести различные реакции протонирования (присоединения протона к какой-либо частице — донору электронов):
а) протонирование молекулы аммиака
 |
Заряд атома азота в катионе аммония Z N = 5-0-4 = +1.
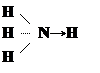 Координационную связь можно изобразить в виде стрелки, направленной от донора к акцептору:
Координационную связь можно изобразить в виде стрелки, направленной от донора к акцептору:
Однако в действительности все четыре связи в ионе аммония совершенно не различимы.
б) протонирование молекулы воды

Заряд атома кислорода в катионе гидроксония: ZO = 6-2-3= +1.
в) протонирование молекулы спирта (метанола)
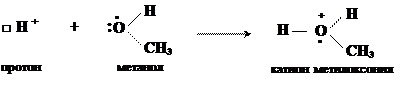 |
Катионы, в которых положительный заряд находится на атоме кислорода носят общее название катионов оксония.
Заряд атома кислорода в катионе оксония: ZО = 6 – 2 – 3 = +1.
3. Анион, владеющий НЭП (донор электронов), взаимодействует с нейтральной молекулой, имеющей свободную орбиталь (акцептор электронов). В результате реакции образуется анион, у которого отрицательный заряд формально принадлежит атому-акцептору:
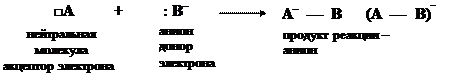 |
Благодаря образованию координативной связи атом-донор нейтрализует свой заряд, а акцептор заряжается отрицательно. Суммарный заряд не изменяется.
Примеры:
а) взаимодействие фторид-аниона и молекулы фторида бора
 |
Заряд атома бора в анионе (BF4)¯ : ZВ = 3-0-4 = -1.
б) взаимодействие молекулы хлорида алюминия и аниона хлора
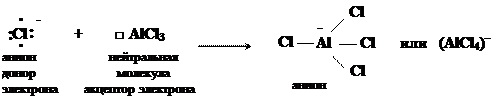
Заряд атома алюминия (AlCl4)¯ : ZAl = 3-0-4 = -1.
4. И свободная орбиталь и неподелённая электронная пара принадлежат нейтральным молекулам. Взаимодействие между ними приводит к образованию новой нейтральной молекулы, но атомы, выступающие и в качестве донора, и в качестве акцептора, получают заряды с противоположными знаками:
 |
Ковалентная связь, образование которой сопровождается появлением разноимённых зарядов на соседних атомах, представляет собой сочетание ковалентной и ионной связей и называется семиполярной или полуионной связью (приставка «семи» означает «наполовину»).
Примеры:
а) взаимодействие молекул аммиака и фторида бора
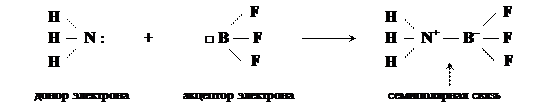 |
ZN = 5-0-4 = +1, ZB = 3-0-4 = -1.
Если семиполярную связь изображают с помощью стрелки, то заряды на атомах не ставятся, но мы их всегда должны иметь в виду: Н3N → BF3.
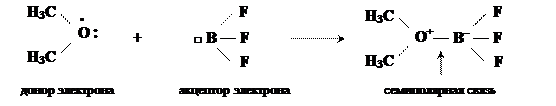 б) взаимодействие диметилового эфира (метоксиметана) с фторидом бора
б) взаимодействие диметилового эфира (метоксиметана) с фторидом бора
ZO = 6-2-3= +1 ZB = -1.
Важным примером соединения, содержащего семиполярную связь, является азотная кислота. Она образуется при каталитическом взаимодействии азотистой кислоты и атомарного кислорода:
Уравнение реакции (без деталей).
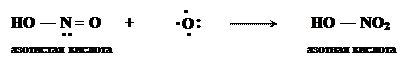 |
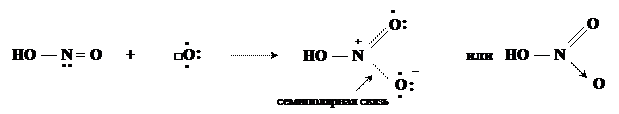 Донором электронной пары является атом азота, акцептором — атом кислорода, который освобождает для этого одну р-орбиталь, спаривая два электрона. Энергия, затраченная на этот процесс компенсируется при образовании новой связи.
Донором электронной пары является атом азота, акцептором — атом кислорода, который освобождает для этого одну р-орбиталь, спаривая два электрона. Энергия, затраченная на этот процесс компенсируется при образовании новой связи.
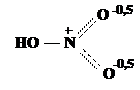 Формально атомы кислорода в нитрогруппе имеют разные заряды. Но фактически здесь происходит процесс делокализации электронов, заряды на атомах кислорода выравниваются, каждый атом реально имеет заряд – 0,5. Атом азота сохраняет заряд +1:
Формально атомы кислорода в нитрогруппе имеют разные заряды. Но фактически здесь происходит процесс делокализации электронов, заряды на атомах кислорода выравниваются, каждый атом реально имеет заряд – 0,5. Атом азота сохраняет заряд +1:
Ваша оценка?