Молекулы воды подвержены диссоциации
H2O = H+ + OH-
В согласии с законом действующих масс выражение для константы равновесия принимает вид
[H+]×[OH-]
K= ¾¾¾¾¾
[H2O]
В 1 л (m=1000 г) воды (молекулярный вес которой М=18 г) содержится n=m/M=1000/18=55.5 молей. Следовательно, концентрация воды в воде равна [H2O]=55.5 моль/л.
Опыт показывает, что произведение К× [H2O]=10-14, поэтому можно записать
[H+]×[OH-]=10-14
Это произведение называют ионным произведением воды и обозначают так
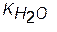 , т.е.
, т.е.
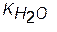 =[H+]×[OH-]
=[H+]×[OH-]
Запомним, что 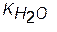 =10-14.
=10-14.
При диссоциации молекул воды H+ ионы и OH- анионы образуются в равных количествах, т.е. в чистой воде [H+]=[OH-]. Следовательно,
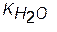 =[H+]2
=[H+]2
поэтому [H+]=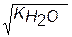 и рН= -1/2lg(
и рН= -1/2lg(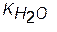 )=7.
)=7.
Итак, в чистой воде концентрации Н+ и ОН- ионов равны, поэтому вода является нейтральной средой, которой соответствует рН=7.
Добавление к воде молекул кислоты увеличивает концентрацию ионов водорода, снижая рН. Следовательно, все кислые растворы имеют рН<7.
Добавление к воде ОН- ионов должно приводить к снижению концентрации ионов водорода, т.к.
[H+]=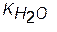 /[OH-]
/[OH-]
Следовательно, все щелочные растворы имеют рН>7 .
Ваша оценка?




