- Классификация спиртов
- По количеству гидроксогрупп
- По типу атома углерода, с которым связана гидроксогруппа
- По строению углеводородного радикала
- Особенности многоатомных спиртов
- Информация об этиленгликоле
- Использование глицерина
- Свойства
- Химические свойства многоатомных спитров
- Кислотные свойства
- Взаимодействие со свежеосажденным гидроксидом меди (II)
- Окисление йодной кислотой и ее солями
- Образование эфиров с азотной кислотой
- Физические свойства спиртов
- Общепринятые свойства
- Получение многоатомных спиртов
- Получение фенола
- Получение альдегидов и кетонов
- Получение карбоновых кислот
- Область применения
- Промышленное применение
- Влияние многоатомных спиртов на человека. Польза и вред
Классификация спиртов
Спирты классифицируют по различным признакам: по количеству гидроксильных групп; по типу атома углерода, с которым связана гидроксогруппа; а также по строению углеводородного радикала.
По количеству гидроксогрупп
По этому признаку выделяют одноатомные и многоатомные спирты.
У одноатомных спиртов одна группа ОН−. Пример — этиловый спирт (этанол):
CH3—CH2—OH(C2H5OH).
У многоатомных — несколько групп ОН−.
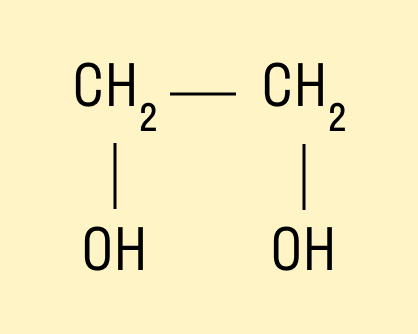
Например, предельный двухатомный спирт этиленгликоль (этандиол):
HO—CH—CH—OH.
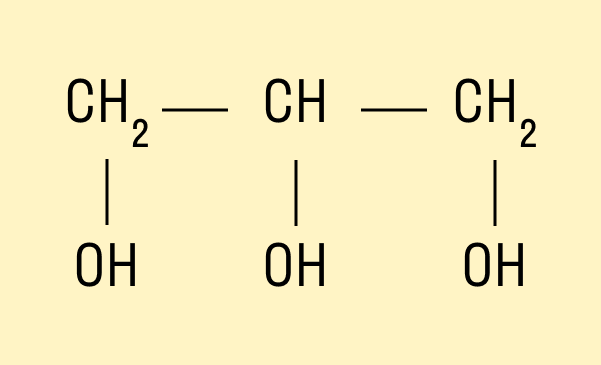
Трехатомный спирт глицерин:
HO—CH2—CH(OH)—CH2—OH.
Современное название многоатомных спиртов — полиолы (диолы, триолы и т. д.).
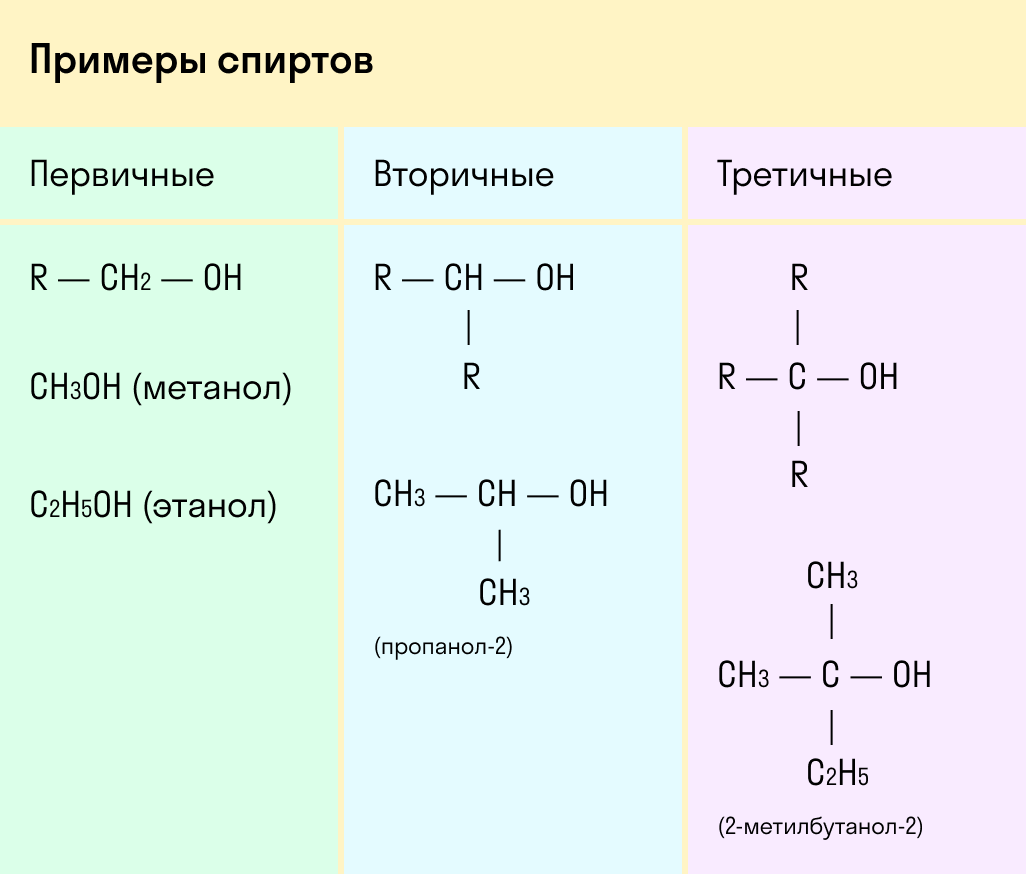
По типу атома углерода, с которым связана гидроксогруппа
Выделяют первичные, вторичные и третичные спирты. Показали примеры каждого вида спиртов в таблице.
По строению углеводородного радикала
По строению углеводородного радикала спирты бывают:
- Предельные (этанол СН3—СН2—ОН);
- Непредельные (пропенол СН2=СН—СН2—ОН);
- Ароматические (фенилметанол С6Н5—СН2ОН).
Особенности многоатомных спиртов
Один из важных представителей многоатомных спиртов — двухатомный этандиол-1,2. Это этиленгликоль. Дополнительно выделяют трёхатомный пропантриол-1,2,3 — глицерин. Отличия заключаются в -ОН в молекулах — изомерия и номенклатура. Эти вещества служат в качестве основных, чтобы создавать другие структурные соединения четырёхатомных и пятиатомных спиртов. Общая формула спирта: CH2OH.
Информация об этиленгликоле

Этиленгликоль является двухатомным спиртом, который не содержит в своём составе примеси. Он полностью прозрачный, его консистенция маслянистая. Если брать другие спирты, этиленгликоль по своим физическим свойствам не имеет специфического и постороннего запаха.
Жидкость обладает сладким вкусом, но к употреблению в пищу запрещена. Если этиленгликоль попадает в организм или на поверхность кожи, появляются повреждения в виде раздражения и ожогов. В медицинской практике есть случаи, когда это соединение приводило к летальному исходу. При внутреннем употреблении в организм попадает повышенное количество токсинов. Этиленгликоль используется в промышленном хозяйстве, продаётся в свободном доступе в специализированных компаниях.
Область применения:
- изготовление топлива для авиационных судов (основная задача заключается в предотвращении обводнения);
- производства взрывчатых веществ на основе нитрогликоля;
- заправка станций, которые занимаются добычей газа в водной среде;
- пропиленгликоль добавляют в крем для обуви, чтобы предотвратить его высыхание при контакте с воздухом.
Это вещество замерзает только при сильном морозе, когда температура воздуха опускается до -65 градусов Цельсия. Соединение имеет свойство самовоспламеняться при определённых условиях. В стандартной окружающей среде вещество полностью безопасное. Отравление организма происходит при регулярном вдыхании паров вещества.
Использование глицерина
Глицерин является органическим соединением и относится к категории трёхатомных спиртов. Это прозрачная жидкость, которая обладает сладковатым вкусом. Вещество нетоксичное для человека, в отличие от других двухатомных спиртов. Глицерин имеет свойство впитывать влагу из окружающей среды. Его можно смешивать в разных пропорциях с этанолом, ацетоном, метанолом и водой.
Вещество не растворяется в эфире и хлороформе. Когда происходит смешивание, выделяется тепло. Раствор уменьшается в объёме. Глицерин находит применение в пищевой промышленности, в процессе производства табачных изделий, электронных сигарет.
В медицине изготавливают лекарственные препараты. Глицерин добавляют в моющие и косметические средства. Его применяют в промышленности, а также для изготовления пластмассы, лаков и красок, электротехнических деталей. Вещество является хорошим функциональным стабилизатором, который сохраняет и увеличивает предельную степень вязкости.
Свойства
Химические свойства многоатомных спиртов обусловлены нахождением в молекуле нескольких гидроксильных групп. Их близкое положение способствует более лёгким разрывам водородных связей, чем у одноатомных спиртов. Многоатомные спирты проявляют кислотные и основные свойства.
Основные химические свойства описаны в таблице.
| Реакция | Описание | Уравнение |
| Со щелочными металлами | Замещая атом водорода в группе -ОН атомом металла, образуют соли с активными металлами и их щелочами |
|
| С галогеноводородами | Одна из групп -ОН замещается на галоген | HO-CH2-CH2-OH + HCl → Cl-CH2-CH2-OH (этиленхлоргидрин) + H2O |
| Этерификация | Реагируют с органическими и минеральными кислотами с образованием жиров – сложных эфиров | C3H8O3 + 3HNO3 → C3H5O3(NO2)3 (нитроглицерин) + 3H2O |
| Качественная реакция | При взаимодействии с гидроксидом меди (II) в щелочной среде образуется тёмно-синий раствор | HO-CH2-CH2-OH + Cu(OH)2 → C4H10O4 + 2H2O |
Соли двухатомных спиртов называются гликолятами, трёхатомных – глицератами.
Химические свойства многоатомных спитров
- Многоатомные спирты более сильные кислоты, чем одноатомные спирты (большее количество гидроксильных групп, кроме того, они оказывают взаимное влияние друг на друга).
Гликоли и глицерины образуют алкоголяты, аналогично одноатомным спиртам. Отличительным свойством является образование соединений типа хелатов с ионами тяжелых металлов. С Cu(ОН) 2 образуется раствор ярко-синего цвета — качественная реакция на многоатомные спирты.
Кислотные свойства
Многоатомные спирты взаимодействуют с щелочными металлами:
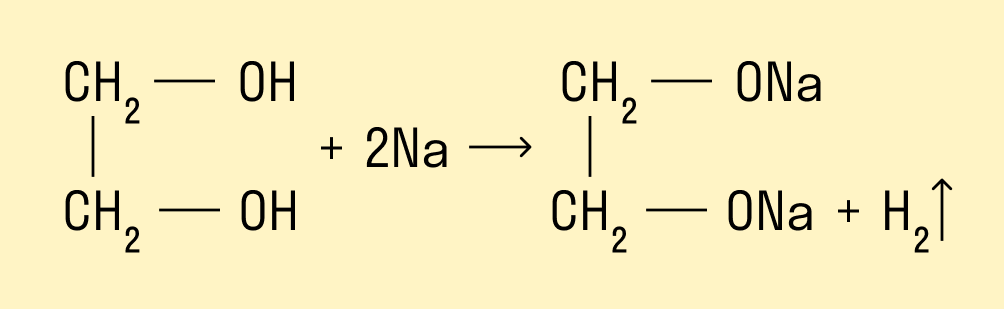
Взаимодействие со свежеосажденным гидроксидом меди (II)
Это качественная реакция на многоатомные спирты:
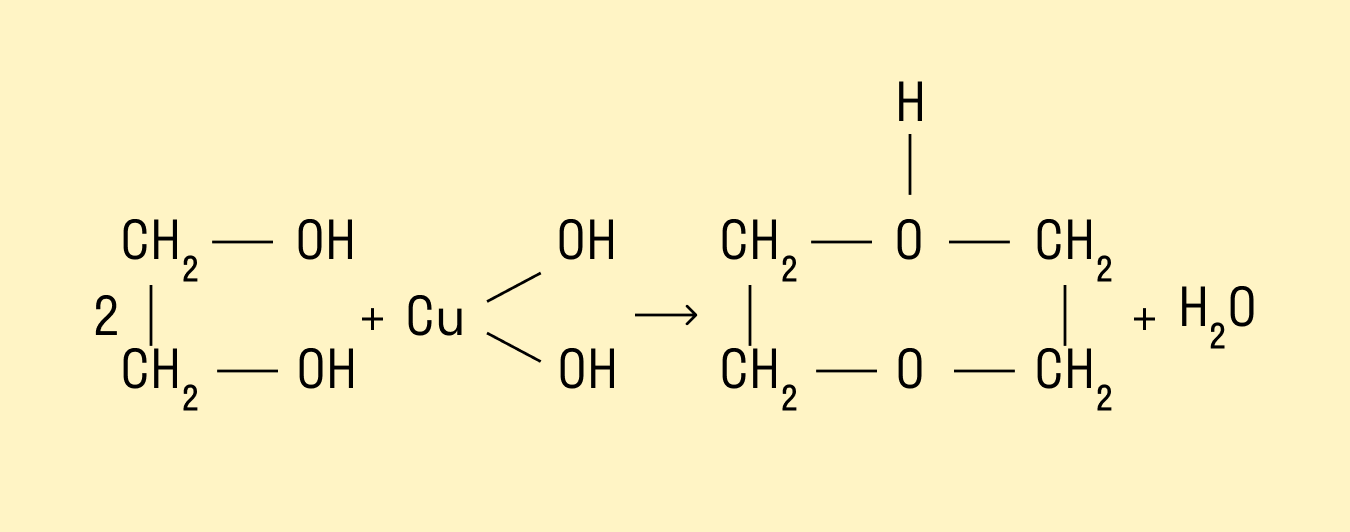
Окисление йодной кислотой и ее солями
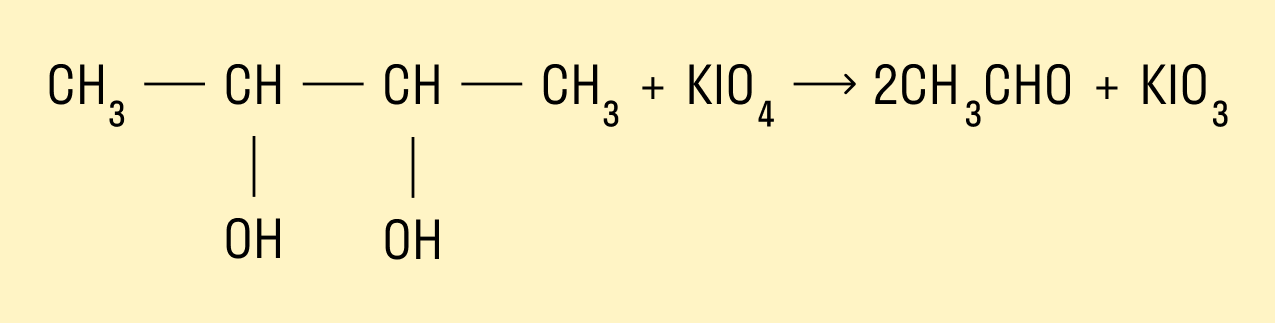
Образование эфиров с азотной кислотой

Физические свойства спиртов
Спирты растворимы в большинстве органических растворителей, первые три простейших представителя – метанол, этанол и пропанол, а также третичный бутанол (Н3С)3СОН – смешиваются с водой в любых соотношениях. При увеличении количества атомов С в органической группе начинает сказываться гидрофобный (водоотталкивающий) эффект, растворимость в воде становится ограниченной, а при R, содержащем свыше 9 атомов углерода, практически исчезает.
Благодаря наличию ОН-групп между молекулами спиртов возникают водородные связи.
В результате у всех спиртов более высокая температура кипения, чем у соответствующих углеводородов, например, Т. кип. этанола +78° С, а Т. кип. этана –88,63° С; Т. кип. бутанола и бутана соответственно +117,4° С и –0,5° С.
Общепринятые свойства
Многоатомные спирты являются органическими веществами, поэтому в сочетании углекислого газа и воды они имеют свойство гореть. В результате происходит выделение большого количества тепла. Его применяют в лабораторных условиях для горелок, чтобы проводить опыты и исследования.

Низшие спирты имеют бесцветное пламя, а высшие — жёлтый оттенок, потому что углерод сгорает не полностью. В реакции со щелочным металлом происходит образование алкоголята натрия. По внешнему виду он напоминает обычную соль. Вещество слабой кислоты, легко вступает в гидролиз. Алкоголят неустойчив при сочетании с водой, потому что происходит процесс разложения на щёлочь и спирт.
Спирты не окисляются при контакте с воздухом. Этот процесс происходит в результате нагревания. В качестве примера можно выделить оксид меди, марганцовку, хромовую смесь. В зависимости от строения исходного спирта и воздействия окислителя получаются разные продукты — альдегиды, кетоны. Третичные спирты устойчивы к процессу окисления.
Спирты легко вступают в реакцию, когда используется гидроксид меди. В результате получается прозрачный раствор, который имеет яркий сине-фиолетовый оттенок. Взаимодействие происходит с азотной кислотой.
Получение многоатомных спиртов
Многоатомные спирты – органические соединения нескольких гидроксильных групп с углеводородным радикалом.
Двухатомные в лаборатории получают:
- Гидролизом галогеналкана, если в молекуле содержится два и более атома галогена.
- Окислением алкенов водным раствором пермангоната калия.
Получение трехатомных спиртов (глицерина) производится кислотным гидролизом животного или растительного жира.
Кроме кислотного гидролиза для получения трехатомного спирта применяют щелочной гидролиз триглицеридов и синтетический метод, основанный на синтезе из полипропилена. Последние два метода применяются в производственных и в лабораторных условиях.
Получение фенола
Фенолы – кислородосодержащие соединения, производные ароматических углеводородов, в которых атомы водорода замещены гидроксильными группами.
В лабораторных условиях фенолполучают гидролизом солей диозония. Соли диозония получают методом воздействия на анилин раствора нитрата натрия в серной или соляной кислоте. Синтез фенола из соединения происходит при кипячении кислого раствора.
Получение альдегидов и кетонов
Альдегиды и кетоны – это два вида карбонильных органических соединений, в молекулах которых содержится карбонильная группа — — С=O. У первых группа связана с атомом водорода и образует альдегидную группу, а у вторых – с двумя углеводородными радикалами образует кетонную группу.
Классическим способом получения альдегидов и кетонов считается окисление спиртов. В обоих случаях используются сильные окислители: перманганат калия, растворенный в серной кислоте, оксид меди. Синтез проходит под воздействием высоких температур.
В процессе окисления первичного спирта происходит синтез альдегида:
Реакцией окисления вторичного спирта получают кетон:
В лаборатории получают карбонильные соединения методом щелочного гидролиза дигалогеналканов. Воздействием водных щелочных растворов на дигалогензамещенные углеводороды, в которых два атома галогена содержатся у одного атома углерода, образуются двухатомные спирты. Полученные вещества проявляют неустойчивость, и при отщеплении воды превращаются в карбонильные соединения.
Альдегиды образуются в случае связи двух атомов галогена с первичным атомом углерода:
При расположении атомов галогена у вторичного атома углерода в процессе гидролиза образуются кетоны:
Получение карбоновых кислот
В лабораториях карбоновые кислоты получают:
- Окислением первичных спиртов кислотными растворами калия перманганата и дихромата калия:
- Окислением альдегидов. Реакция проходит по методике и с использованием реагентов, примененных в окислении спиртов:
R-CHO + [O] ⟶R-COOH
Аналогичная реакция проходит с окислением альдегида оксидом серебра или гидроксидом меди:
R-CHO + Ag2O ⟶R-COOH + 2Ag—
R-CHO + 2Cu(OH)2 ⟶R-COOH + Cu2O— + 2H2O
Опыт по получению органических кислородосодерожащих соединений в лабораторных условиях закрепляют теоретических навыки и создает необходимую базу для внедрения в производство новых технологий.
Область применения
Многоатомные спирты находят широкое применение в повседневной жизни. Можно выделить следующие варианты использования:
- Этиленгликоль (HO-CH 2 -CH 2 -OH). Вещество применяется для изготовления лавсана или для производства антифриза. Это водные растворы, которые замерзают при -20 градусах Цельсия. Их применяют для охлаждения двигателя, поэтому транспортное средство эксплуатируется в зимнее время года. Этиленгликоль применяют в качестве сырья при органическом синтезе.
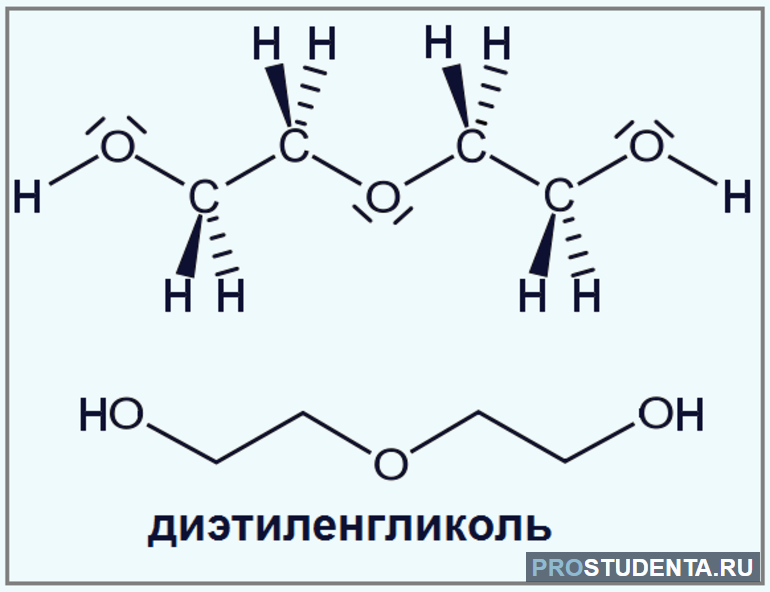
- Диэтиленгликоль (C4H10O3). Его используют для заполнения системы тормозных гидравлических приспособлений. Вещество активно применяется в текстильной промышленности на этапе отделки, придания оттенка ткани.
- Глицерин (C 3 H 5 (OH) 3). Он нашёл широкое применение в разных сферах — парфюмерия, пищевая, текстильная промышленность. Глицерином обрабатывают ткань или кожу, чтобы она сохраняла свои первоначальные свойства.
- Нитроглицерин (C3H5N3O9). Для его производства используют глицерин. Это хорошее сырьё, которое применяют, чтобы получить бездымный порох или динамит. Готовая продукция используется для строительства железных дорог. Нитроглицерин в чистом виде взрывается даже при незначительном ударе, является токсичным веществом. В минимальном количестве — это лекарственное средство для расширения сосудов, улучшения кровоснабжения сердечной мышцы.
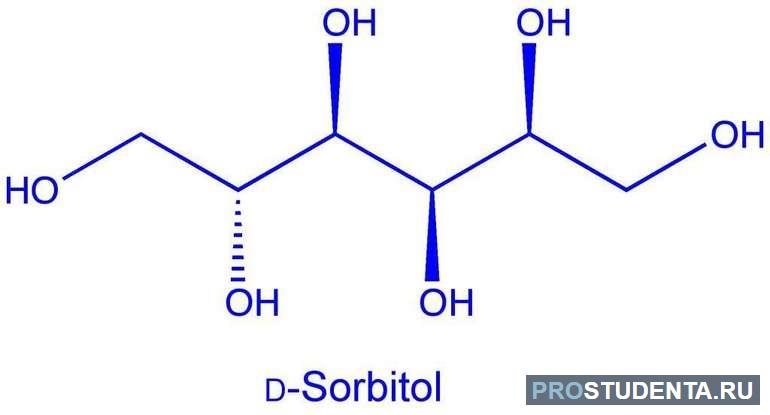
- Сорбит (C 6 H 8 (HO) 6). Его ещё называют глюцитом. Это шестиатомный спирт, который имеет сладкий вкус. Его применяют для изготовления аскорбиновой кислоты. Сорбит — пищевая добавка Е420, которую применяют в качестве заменителя сахара для больных диабетом. Его можно встретить в различных диетических продуктах и напитках.
- Ксилит (CH 2 OH (CHOH) 3 CH 2 OH). Имеет вид сладких кристаллов, которые легко и быстро растворяются при контакте с водой. Применяют для производства продуктов питания людям с сахарным диабетом. Вещество нашло широкое применение при изготовлении олифы, алкидной смолы, поверхностно-активного вещества.
Эти спирты обладают уникальными свойствами. Благодаря этому их применяют в разных сферах промышленности и в бытовых целях.
Промышленное применение
Полиспирты используют практически во всех промышленных сферах. Удивительно применение одних и тех же веществ в очень далеких друг от друга отраслях. Так, глицерин используют в косметологии и в изготовлении взрывчатых веществ. Без полиолов невозможно производство пластмасс, лакокрасочных материалов, полиуретанов, термоактивных полимерных смол, антифризов.
В производстве пластмасс полиспирты позволяют повысить упругость, устойчивость к деформации, увеличить долговечность изделий.
Особенно интересует потребителей информация об использовании многоатомных спиртов в пищевой промышленности. Эти вещества обладают уникальными свойствами, позволяющими добавлять их в еду для достижения сладкого вкуса. Полиолы — это отличные сахарозаменители, которые при этом имеют множество положительных качеств:
- нетоксичны;
- полностью усваиваются организмом человека;
- низкокалорийны;
- не вызывают кариес;
- можно употреблять больным диабетом.
Использование в пищу спиртов не требует для усвоения выделения инсулина, поэтому особенно важным является возможность их применения в изготовлении диабетической продукции. Так, с использованием полиспиртов выпускают жевательную резинку, шоколад, газированные напитки, диабетические сладости.
Часть сахарозаменителей имеют полезные свойства, не относящиеся к способности придавать сладость продуктам. Так, глюцит (второе название сорбита) используется в фармакологии в качестве ароматизатора и загустителя для жидких лекарственных форм. Ксилит включают в состав раствора для внутривенного питания.
Также сорбит используют как гигроскопичное вещество при изготовлении мясных полуфабрикатов для увеличения срока годности продукта. Это же свойство удерживать влагу позволяет использовать сорбит в косметологии при производстве кремов, лосьонов и зубной пасты.
Влияние многоатомных спиртов на человека. Польза и вред
С увеличением интереса к правильному питанию появляется интерес потребителя к информации о полиолах. Что это такое, вредно или нет, хотят знать многие. Говоря о пользе и вреде многоатомных спиртов, в первую очередь нужно рассматривать вещества, используемые в качестве пищевых добавок.
Как уже было сказано выше, сорбит, ксилит и изомальт являются средствами, заменяющими сахар в продуктах. При этом очевидна их польза в качестве антибактериальных, диабетических, диетических и профилактических добавок. Сорбит и ксилит при этом оказывают положительное влияние на перистальтику кишечника и используются в качестве щадящего слабительного средства.
Отрицательное воздействие на организм человека зависит от количества и периодичности употребления. Постоянный прием в больших дозах сахарозаменителей на основе полиолов способен спровоцировать дисбаланс в ЖКТ, обострить холецистит, вызвать тошноту, головные боли. Применять сахарозаменители людям, страдающим печеночной или почечной недостаточностью, болезнями ЖКТ и хроническим гепатитом, не рекомендуется.
Ксилит представляет собой смертельную опасность для собак. Организм животного принимает даже минимальную дозу вещества за сахар и запускает мощный выброс инсулина. Результатом становится гликемия с печальным прогнозом.
- https://skysmart.ru/articles/chemistry/spirty
- https://ProStudenta.ru/article-2926.html
- https://obrazovaka.ru/himiya/mnogoatomnye-spirty-formula-stroenie.html
- http://himege.ru/mnogoatomnye-spirty-poluchenie-ximicheskie-svojstva/
- https://www.krugosvet.ru/enc/nauka_i_tehnika/himiya/SPIRTI.html
- https://bingoschool.ru/manual/osnovnyie-sposobyi-polucheniya-organicheskix-kislorodosoderzhashhix-soedinenij/
- https://vkmp.ru/promyshlennost/14552-polioly-jeto-mnogoatomnye-spirty-polispirty-svojstva-proizvodstvo-i-primenenie/
Ваша оценка?