- Что такое альдегиды
- Описание веществ
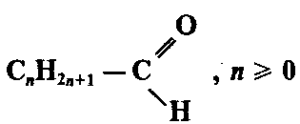
- Общая формула альдегидов
- Строение альдегидов и кетонов
- Карбонильная группа
- Общая структура молекул альдегидов и кетонов
- Характерные запахи альдегидов
- Примеры альдегидных композиций
- Свойства альдегидов
- Химические свойства
- Физические свойства
- Предельные (насыщенные) альдегиды
- Гомологический ряд
- Номенклатура и изомерия
- Изомерия кетонов и альдегидов
- Позиция функциональной группы
- Строение углеродного скелета
- Межклассовая изомерия
- Получение
- Получение и применение альдегидов на примере уксусного альдегида
- Реакции присоединения
- Реакции конденсации
- Качественные реакции
- Где и как используются альдегиды
Что такое альдегиды
В дебрях химии можно отыскать официальное определение альдегидов:
Альдегиды — это отдельный класс неких органических соединений, в которых обязательно содержится группа –CHO, т.н. «альдегидная группа». Это вещества типа «R-CHO», где карбонильная группа прямо связана с атомом водорода (одним) и группой R (тоже одной).
Но если карбонильные, СНО-содержащие группы звучат для вас, как Шицзячжуанский диалект, давайте максимально упростим. Но сначала договоримся:
- Во-первых, альдегиды вообще и альдегиды, как парфюмерный термин – это не одно и то же. В парфюмерии группа альдегидов представляет собой более сжатое понятие. Если максимально упрощать, а именно это мы и договорились делать в данной статье, то парфюмерные альдегиды должны пахнуть.
- Во-вторых, пройдемся по основным понятиям, которые предлагают нам различные источники, и, определив, что из них является мифом, отставим только правду, что и будет упрощенной версией.
- В-третьих, с научной точки зрения, разные вещества в парфюмерии могут являться альдегидами, но нам, как пользователям ароматов, важно понимать, что подразумевается под этим понятием в описании композиций. Увидели в составе альдегиды, и не вспоминаете химию, а примерно представляете, о чем идут речь.
Завершающий пункт может быть пока не до конца понятным, но просто запомните его, далее все встанет на свои места.
Описание веществ
Альдегиды в отличие от спиртов не обладают подвижным атомом водорода, поэтому их молекулы не ассоциируются, что объясняет значительно более низкие температуры кипения. К примеру, альдегид формальдегид кипит уже при температуре -21 °С, а спирт метанол – при +65 °С.
Однако такой низкой температурой кипения обладает только формальдегид, следующий представитель – ацетальдегид закипает при +21°С. Поэтому при комнатной температуре из всех альдегидов только формальдегид – газ, ацетальдегид уже легколетучая жидкость. Увеличение количества атомов углерода закономерно повышает температуру кипения. Так, бензальдегид С6Н5СНО закипает только при +180 °С. Разветвление цепи вызывает понижение температуры кипения.
Низшие альдегиды, к примеру, формальдегид, хорошо растворимы в воде. 40%-ный раствор формальдегида называют формалином, его часто используют для консервации биологических препаратов. Высшие альдегиды хорошо растворимы в органических растворителях – спирте, эфире.
Общая формула альдегидов
Общая формула альдегидов: R–CН=O,
где R – атом водорода или углеводородный радикал.
Общая формула предельных альдегидов – СnH2nO или CnH2n+1–CH=O
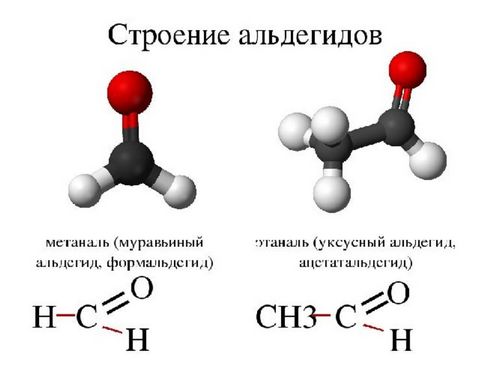
Строение альдегидов и кетонов
Определяющий элемент структуры производных углеводородов – функциональная группа атомов. Она служит критерием для отнесения соединения к тому или иному классу органических веществ.
Формальгид – простейший альдегид, имеет молекулу, связанную с двумя атомами водорода. У всех других альдегидов молекулы связаны лишь с одним атомом водорода.
Углерод, связанный с карбонильной группой может быть частью алкильных либо неалкильных групп, они в свою очередь могут быть ациклическими, ароматическими или гетероциклическими кольцами. Органические соединения, обладающие двумя альдегидными группами называются диальдегидами.
Карбонильная группа
Группа называется карбонилом. Она образована посредством двойной связи, поскольку оба входящих в ее состав атома – углерод и кислород – sp2-гибридизованы.
В карбонильной группе атом углерода затрачивает на связь одну из трех валентностей, образованных гибридными sp2-облаками, и на связь – валентность, создаваемую единственным негибридным 2p-облаком. Кислородный атом вступает в связь с углеродом, затрачивая единственную свободную гибридную орбиталь, и в связь – через 2p-орбиталь аналогично углероду. Два оставшихся гибридных облака кислорода содержат неподеленные электронные пары и не создают свободных валентностей.
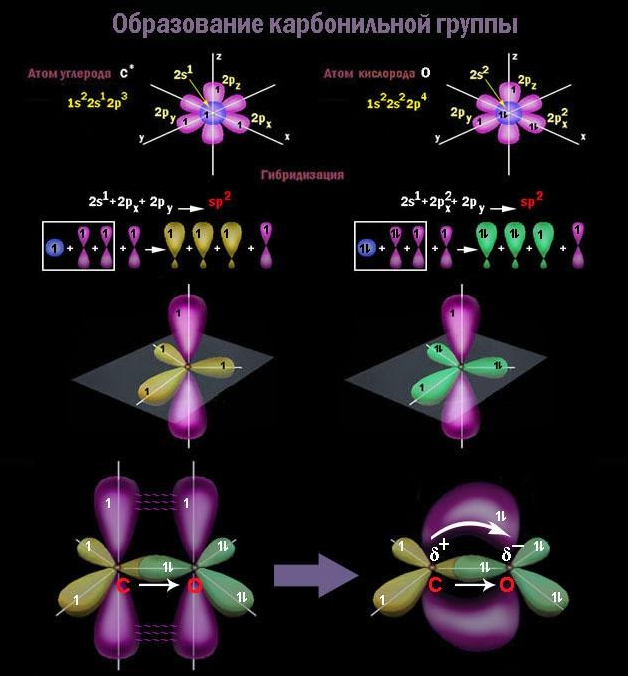
Благодаря высокой электроотрицательности кислород оттягивает в свою сторону электронную плотность по обоим компонентам двойной связи, и она оказывается сильно поляризованной. За счет электронов, обладающих большой подвижностью и легко смещающихся к кислороду, дипольный момент связи C=O почти вчетверо выше, чем у одинарной связи С-O, характерной для спиртов.
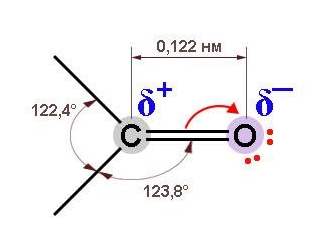
На диполе C=O кислород обладает частичным отрицательным, а углерод – положительным зарядом. Это приводит к поляризации связей С-O у соседнего с карбонилом углеродного атома (отрицательный индуктивный, или I-эффект) и оказывает влияние на химические свойства.
Общая структура молекул альдегидов и кетонов
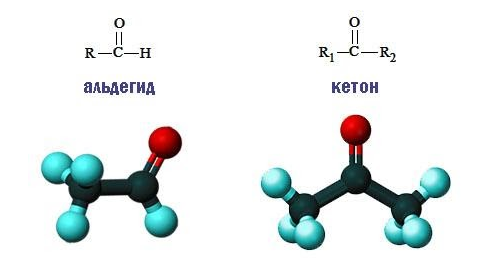
Состав карбонильных соединений описывается общей формулой. Различия между альдегидами и кетонами состоят в разном строении углеводородных остатков.
В альдегидах одна из свободных валентностей углерода группы присоединяет алкильный радикал, а вторая – атом водорода. В кетонах обе валентности связывают карбонил с алкильными остатками. Общее строение молекул соединений обоих классов имеет следующий вид:
Характерные запахи альдегидов
Альдегиды обладают характерными запахами, причем низшие – резкими, неприятными. Всем известен неприятный запах формалина – водного раствора формальдегида. У высших альдегидов цветочные запахи, их применяют в парфюмерии.
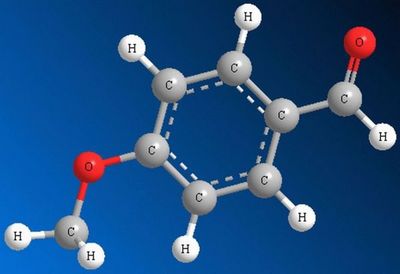
Примером альдегидов – веществ с приятным запахом — является ванилин, обладающий ароматом ванили, и бензальдегид, придающий характерный аромат миндальным орехам. Оба вещества получают синтетически и широко используют в качестве ароматизаторов в кондитерской промышленности и парфюмерии.
Примеры альдегидных композиций
Вспоминать еще раз Шанель №5 не будем. Обратим внимание на другие хиты из данной группы парфюмерии.
Женские:
- Lanvin Arpege, 1927 год.
- Climat от Lancome, 1967 год.
- Hermes Amazone, 1974 год.
Мужские:
- Chanel Allure Sport Homme, 2004 год.
- Aramis Aramis, 1966.
- Givenchy Pi, 1998 год.
Конечно, это лишь капля в море альдегидной группы, но очевидно, что практически все старички выпускаются до сих пор, т.е. именно в этом семействе можно создать особых долгожителей. Желающие увидеть все ароматы данной группы могут просто нажать на кнопку:
Свойства альдегидов
Химические свойства
Практически все альдегиды способны вступать в разнообразные химические реакции, включая полимеризацию. Сочетание их с другими видами молекул ведет к созданию так званных конденсационных полимеров, которые активно используются, например, при производстве пластмассы, в качестве растворителей и парфюмерных ингредиентов.
А некоторые альдегиды даже принимают активное участие в физиологических процессах, так они являются частью:
- витамина А, очень важного для зрения,
- пиридоксальфосфата – одной из форм витамина В6,
- глюкозы и прочих редуцированных сахаров,
- некоторых природных и синтетических гормонов.
Важным отличием альдегидов от тех же углеродов является наличие у них карбонильной группы. Карбонильная группа эта изначально полярна, то есть электроны образующие связь С=О притягиваются больше к кислороду, нежели к углероду. Благодаря этому первый из электронов получает отрицательный заряд, а второй положительный.
Также стоит заметить, что альдегиды имеют более высокий дипольный момент по сравнению с остальными углеводородными соединениями.
Физические свойства
Температура кипения альдегидов и их плавления гораздо выше у карбонилсодержащих соединений, нежели у просто состоящих из углерода и водорода. К примеру, бутан и ацетон имея одинаковую молекулярную массу, закипают очень по разному: бутан закипает уже при 0 С, в то время как ацетону для кипения необходимо уже +56 С.
В отличие от углеводородов альдегиды способны растворятся в воде, но не все, а только имеющие менее пяти атомов углерода в молекуле. Но если углеводородная часть их молекул выше этого числа, это делает их нерастворимыми в воде.
Предельные (насыщенные) альдегиды
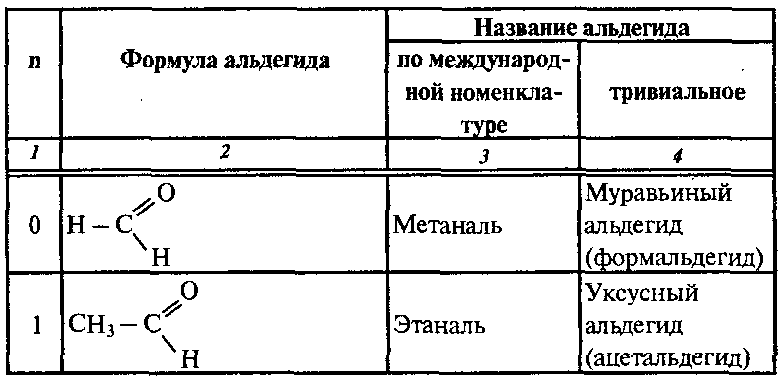
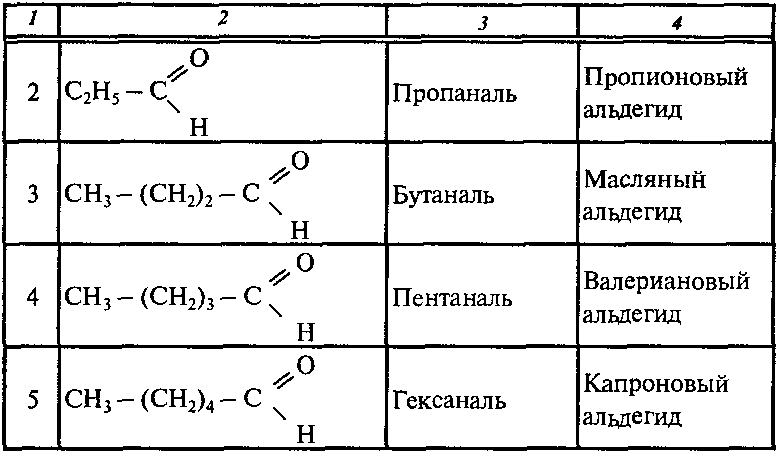
Гомологический ряд
Номенклатура и изомерия
Название альдегида по международной номенклатуре образуется от названия соответствующего алкана с таким же числом атомов углерода с добавлением окончания –аль. Нумерацию углеродной цепи начинают от атома углерода альдегидной группы.
В пределах класса альдегидов возможен только один вид изомерии – изомерия углеродной цепи.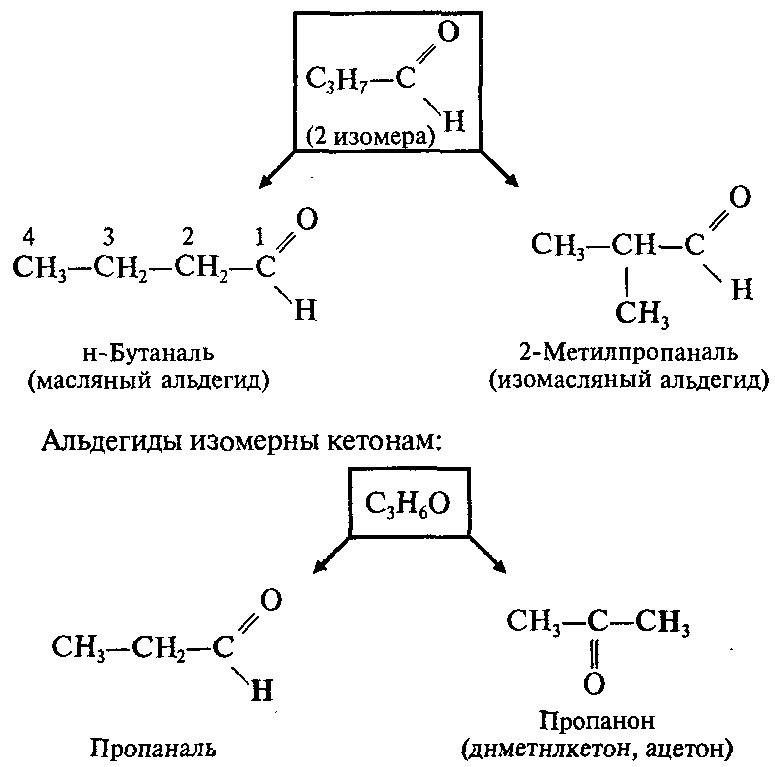
Изомерия кетонов и альдегидов
Соединения состава образуют изомеры по структурным признакам: строению образующей молекулу углеродной цепи, местоположению карбонильных групп и наличию изомеров в других классах органических веществ.
Позиция функциональной группы
Изомерия данного типа свойственна кетонам с:

Строение углеродного скелета
Изомерия по отсутствию либо наличию и характеру ветвления углеродной цепи свойственна всем карбонильным соединениям: альдегидам с и кетонам с. Ацетальдегид и формальдегид изомеров не имеют.
Например, альдегиды состава образуют изомеры:
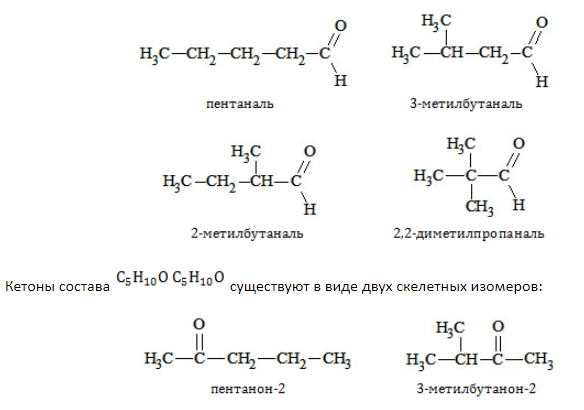
Межклассовая изомерия
Из единой для двух классов соединений общей формулы следует, что альдегиды и кетоны одинакового атомного состава – взаимные изомеры:
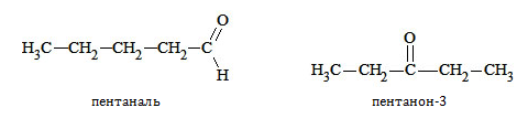
Кроме того, они обладают межклассовой изомерией с такими соединениями, как:
- непредельные спирты – алкенолы (при);
- простые эфиры (при);
- циклические оксиды (при).
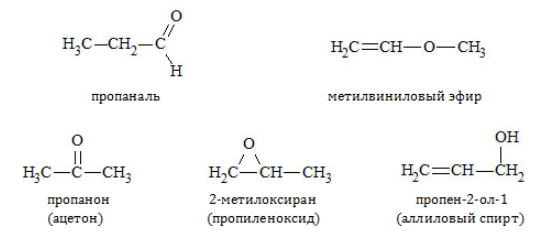
Получение
Рассмотрим способы получения альдегидов.
- Окисление спиртов.
Альдегиды получают при окислении первичных спиртов. Например, формальдегид, который используют в производстве полимерных материалов, лекарств, красителей, взрывчатых веществ. В промышленности формальдегид получают окислением кислородом метанола: 2СН3ОН + О2 = 2СН2О + 2Н2О.
Реакцию проводят на раскаленной серебряной сетке, серебро является катализатором. Через сетку пропускают пары метанола, смешанные с воздухом. Реакция идет с выделением большого количества тепла, которого хватает для поддержания сетки в раскаленном состоянии.
- Дегидрирование спиртов.
Альдегиды можно получать из спиртов и в отсутствии кислорода. В этом случае используют медный катализатор и высокие температуры (250 °С): R-CH2-OH = R-CHO + H2.
- Восстановление хлорангидридов кислот.
Альдегиды можно получать восстановлением водородом хлорангидридов кислот. В качестве катализатора используют «отравленный» палладий – с пониженной активностью: RCClO + H2 = RCHO + HCl.
- Получение ацетальдегида.
Ацетальдегид в промышленности получают окислением этилена кислородом или воздухом в жидкой фазе. В качестве катализатора необходим хлорид палладия (PdCl2): 2 СН2=СН2 + О2 = 2 СН3 СНО.
Получение и применение альдегидов на примере уксусного альдегида
Уксусный альдегид получают в больших количествах при помощи реакции Кучерова*:
* Кучеров Михаил Григорьевич (3.06.1850–26.06.1911) — русский химик-органик, открыл (1881) реакцию каталитической гидратации ацетиленовых углеводородов с образованием карбонилсодержащих соединений.
В небольших количествах этот альдегид можно получить окислением этанола:
Задание 23.5. В уроках 20.3 и 22.4 посмотрите на соответствующие уравнения реакций; обратите внимание, за счёт каких атомов они происходят, и попробуйте составить аналогичные уравнения реакций:
- пропин + вода →
- пропанол-1 + СuО →
- пропанол-2 + СuО →
Сделайте вывод: всегда ли в этих реакциях получаются альдегиды?
Если Вы всё сделали правильно, в реакциях 1 и 3 получается ацетон (кетон), а в реакции 2 — пропаналь.
Уксусный альдегид применяют для получения уксусной кислоты, этилового спирта, лекарств и других веществ.

Реакции присоединения
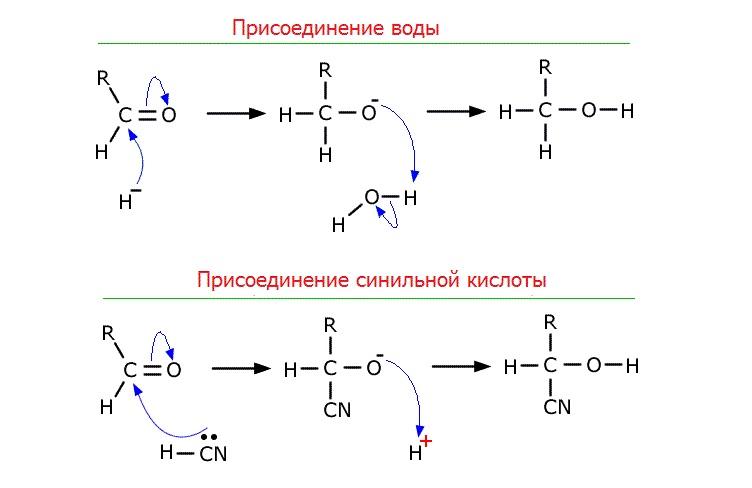
В карбонильной группе С=О электронная плотность смещена к атому кислорода, поэтому на карбонильном атоме углерода формируется частичный положительный заряд, который обусловливает химическую активность альдегидов. Положительный заряд на атоме углерода группы С=О обеспечивает его активность в реакциях с нуклеофильными реагентами – водой, спиртом, магний органическими соединениями. Атом кислорода воды может атаковать карбонильный атом углерода, присоединяться к нему и вызывать разрыв связи С=О.
Реакции конденсации
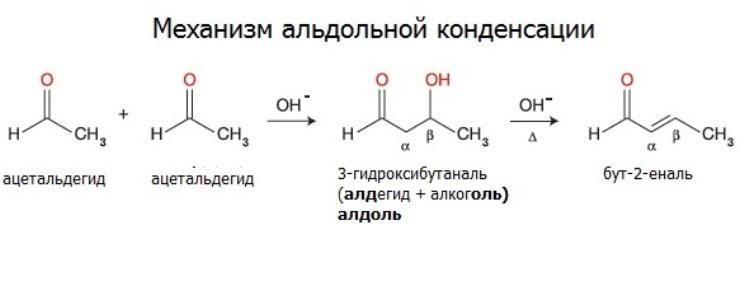
Альдегиды вступают в реакции альдольной и кротоновой конденсации.
Ацетальдегид при действии слабого раствора щелочи на холоду превращается в альдоль. Продуктом реакции является жидкость, смешивающаяся с водой при пониженном давлении. Это вещество содержит как альдегидную, так и спиртовую группу (отсюда и название).
Качественные реакции
Для выявления альдегидов можно использовать две качественные реакции:
- Реакция «серебряного зеркала». Реакция идет с реактивом Толленса – аммиачным раствором оксида серебра. При смешивании раствора аммиака и раствора нитрата серебра образуется сначала раствор гидроксида серебра, а при добавлении избытка аммиака — раствор гидроксида диамминсеребра (I), который и является окислителем. При взаимодействии с альдегидом выделяется элементное серебро в виде черного осадка. Если реакцию проводить при медленном нагревании, не тряся пробирку, серебро покроет стенки пробирки, создавая эффект «зеркала».
- Реакция «медного зеркала». Другим реактивом, открывающим альдегидную группу, является гидроксид меди (II). При взаимодействии с альдегидом он восстанавливается до оксида меди (I). Цвет меняется с синего сначала на оранжевый, затем на желтый. Если реакцию проводить при медленном нагревании, оксид будет образовывать тонкий оранжево-красный налет на стенках пробирки – «медное зеркало»: СН3СНО + 2 Cu(OH)2 + NaOH = CH3COONa + Cu2O↓ + 3H2O.
Где и как используются альдегиды
Альдегиды являются токсичными веществами и обладают способностью накапливаться в организме. Также соединения характеризуются раздражающим и нейротоксическим действием. Эффект определяется молекулярной массой: чем она больше, тем слабее раздражающее, но сильнее наркотическое действие. При этом ненасыщенные альдегиды обладают большей токсичностью по сравнению с насыщенными.
Определенные виды альдегидов имеют канцерогенные свойства. Вещества вызывают раздражение слизистых оболочек глаз и верхних дыхательных путей, негативно влияют на нервную систему. При увеличении количества атомов углерода в молекуле раздражающее действие уменьшается. Ненасыщенные альдегиды обладают более сильным раздражающим действием по сравнению с насыщенными.
Ацетальдегид СН3СНО вызывает возбуждение, которое сменяет наркоз. Вещество представляет собой промежуточный продукт метаболизма этилового спирта в организме. Действие тримера этого альдегида — паральдегида (С2Н4O)3 — мощнее и длительнее. Тетрамер — метальдегид (С2Н4O)4 — представляет собой более токсичное вещество. Увеличение длины алкильного радикала в молекуле альдегида сопровождается усилением физиологической активности и токсичности соединения.
Путем введения галогена в молекулу альдегида усиливают наркотическое (снотворное) действие вещества. Таким образом, наркотические свойства хлораля более выражены, чем у ацетальдегида. Альдегидная группа повышает степень токсичности вещества.
Данный показатель может быть существенно снижен в процессе образования гидратной формы альдегида. Гидратные формы характеризуются низкой токсичностью. В такой форме хлораль используют в медицинской отрасли под названием хлоралгидрата, который проявляет снотворное действие.
Введение гидроксильных групп в молекулу альдегида или их конденсация, сопровождающаяся формированием альдолей, значительно понижают реакционную способность, а также физиологическую активность соединений. К примеру, сахара являются фармакологически инертными веществами.
Ароматические альдегиды в большей степени характеризуются низкой токсичностью, что объясняется простотой их окисления до соответствующих кислот, которые, как правило, достаточно инертны.
Лекарственные препараты, в составе молекулы которых есть альдегидная группа, с указанием их основного действия на организм:
По сравнении с другими альдегидами наибольшими объемами производства характеризуется формальдегид (примерно 6 млн тонн/год). Основной областью применения вещества является выпуск смол — бакелита, галалита (в сочетании с мочевиной, меламином и фенолом). Соединение используют в процессе дубления кож и протравливания зерна.
Также из формальдегида производят лекарственные средства (уротропин). Соединение используют в качестве консерванта биологических препаратов (за счет свойства свертывать белок). Формальдегид является предшественником метилендифенилдиизоцианата, который применяется при изготовлении полиуретанов и гексогена, являющегося достаточно мощной взрывчаткой.
Вторым по объемам производства альдегидом является масляный альдегид. Синтезируют примерно 2,5 млн тонн в год данного вещества по технологии гидроформилирования. Определенные виды альдегидов получают в ограниченных масштабах (менее 1000 тонн в год) и применяют как ингредиенты в парфюмерной промышленности. К примеру, к таким соединениям относят коричный альдегид и его производные в виде цитраля и лилиаля.
Ацетальдегид применяют в процессе получения уксусной кислоты, этилового спирта, бутадиена для синтеза производных пиридина, пентаэритрита и кротонового альдегида, поливинилацетата и пластмасс. Вещества необходимы для производства спиртов, в том числе, бутиловых, 2-этилгексанола, пентаэритрита. Также альдегиды используют для получения карбоновых кислот, полимеров, антиоксидантов, пиридиновых оснований.
- https://vash-aromat.ru/aldegidnaya-parfumeria
- https://FB.ru/article/438739/aldegidyi-primeryi-opisanie-poluchenie-svoystva
- http://ru.solverbook.com/spravochnik/formuly-po-ximii/formula-aldegida/
- https://allinchemistry.ru/organicheskaya-himiya/gomologicheskij-ryad-aldegidov-i-ketonov
- https://www.poznavayka.org/himiya/aldegidyi/
- https://al-himik.ru/aldegidy/
- https://1Ku.ru/obrazovanie/37768-aldegidy-primery-opisanie-poluchenie-svojstva/
- https://himi4ka.ru/samouchitel-po-himii/urok-23-aldegidy.html
- https://Wika.TutorOnline.ru/himiya/class/10/aldegidy-himicheskie-svojstva-poluchenie-primenenie
Ваша оценка?