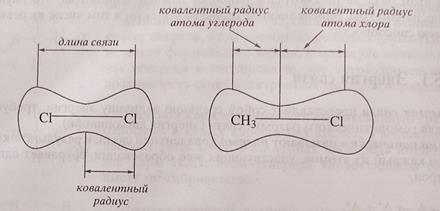
Параметры, характеризующие ковалентные связи, весьма многообразны. Важнейшими из них являются энергия связи, длина связи, полярность, поляризуемость.Длина связи – это расстояние между центрами связанных атомов (r). Поскольку атомы в молекулах колеблются вдоль линий связей, измеряемые расстояния представляют собой средние значения. Длина связи выражается через сумму ковалентных радиусов атомов. Ковалентный радиус – это половина длины ковалентной связи в молекуле, образованной одинаковыми атомами (рис. 28).
|
|
С увеличением порядкового номера элемента ковалентный радиус его атома возрастает, следовательно, увеличиваются и длины связей (табл. 1). Таблица 1.Зависимость длин связей от ковалентных радиусов атомов
| Атом | Ковалентный радиус,нм | Связь | Длина, нм |
| H | 0,030 — 0,037 | C sp3—H | 0,110 |
| Сsp3 | 0,077 | С—С | 0,154 |
| Cl | 0,099 | С—Cl | 0,176 |
| Br | 0,114 | С—Br | 0,194 |
Длины связей с участием атома углерода зависят от способа гибридизации его атомных орбиталей. Для одинарных связей, образованных гибридными орбиталями, длины связей уменьшаются с увеличением доли s-орбитали в гибридной. При увеличении кратности связей между атомами их длина всегда уменьшается (табл.2). Таблица 2.Основные характеристики ковалентных связей (средние значения)
| Тип связи | Гибридизация атома углерода | Длина,нм | Дипольный момент |
| С—С | sp3 | 0,154 | |
| С = С | sp2 | 0,134 | |
| С ≡ С | sp | 0,120 | |
| С—Н | sp3 | 0,110 | 0,30 |
| С—Н | sp2 | 0,107 | 0,40 |
| С—O | sp3 | 0,143 | 0,86 |
| С = O | sp2 | 0,121 | 2,40 |
| С—N | sp3 | 0,147 | 0,45 |
| С = N | sp2 | 0,128 | 1,40 |
| С ≡ N | sp | 0,116 | 3,60 |
| С—Сl | sp3 | 0,176 | 1,47 |
| С—Br | sp3 | 0,194 | 1,42 |
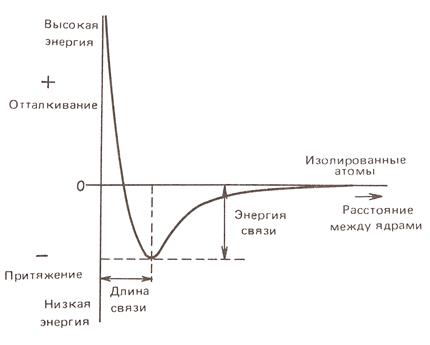
Энергия связи – это та часть энергии, которую необходимо затратить для разрыва связи между двумя атомами, или же та часть энергии, которая выделяется при образовании связи. Энергия разрыва связи противоположна по знаку энергии образования. Экспериментально энергию связи определяют по теплоте сгорания веществ. Между длинной связи и её энергией существует следующая зависимость: чем короче связь, тем больше её энергия, тем связь прочнее, и наоборот. Энергия связи конкретной пары атомов, зависит от валентного состояния атомов.Повышение кратности увеличивает энергию связи. Однако прочность увеличивается не в кратное количество раз, следовательно π-связи менее прочные, чем σ-связи. Структурные особенности молекулы также заметно влияют на величину энергии связи. Например, энергия связи С–Н уменьшается в ряду первичный – вторичный – третичный атом углерода (табл. 3). Таблица 3.Величины энергии важнейших связей
| Связь | Энергия, кДж/моль | Связь | Энергия, кДж/моль |
| С—С | 348 | N—N | 163 |
| С = С | 620 | N ≡ N | 941 |
| С ≡ С | 814 | С—N | 293 |
| С sp3—Н | 414 | C ≡ N | 854 |
| С sp2—Н | 435 | N—H | 390 |
Полярность связи обусловлена неравномерным распределением электронной плотности. Склонность атомов притягивать электроны связи характеризуется их электроотрицательностью (ЭО). Она связана, с одной стороны, со способностью атома удерживать валентные электроны (энергия ионизации атома), а с другой стороны, его способностью притягивать дополнительные электроны (сродство атома к электрону). Поэтому она часто рассматривается как функция двух видов энергии. ЭО элементов увеличивается в периоде слева направо, а в группе – снизу вверх. Наиболее известной шкалой элоктоотрицательности является шкала Л.Полинга.
Ваша оценка?