Электролиз – совокупность процессов, протекающих под действием электрического тока на электродах, которые погружены в раствор или расплав.
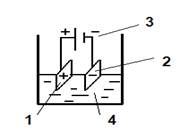
1 – анод;
2 – катод;
3 – источник тока;
4 – ячейка.
Частица из раствора или расплава, находящаяся вблизи отрицательного электрода принимает ē, то есть восстанавливается.
Электрод, на котором происходит процесс восстановления над катодом.
Частицы, находящиеся вблизи положительного электрода отдают ē т.е. окисляются.
Электрод, на котором происходит процесс окисления над анодом.
Существует электролиз растворов и электролиз расплавов. Причем электролиз расплавов применим к щелочам и солям. В качестве инертных электродов применяют платиновые и графитовые электроды. В качестве растворимого анода могут использоваться медные, железные, кобальтовые и др.
Ваша оценка?