Рассмотрим химическое равновесие для реакции образования малорастворимого основания
Men+ + nOH- = MeOH¯
Для этой реакции закон действующих масс принимает вид
1
K = ¾¾¾¾¾
[Меn+][OH-]n
т.к. по соглашению принимается, что для веществ, образующих самостоятельную фазу, концентрация равна 1 ([MeOH]кр=1).
Из этого уравнения следует, что произведение концентраций ионов металла и гидроксила при равновесии должно оставаться постоянной величиной, которую назвали произведением растворимости
ПР= [Меn+][OH-]n
То значение рН, которое отвечает химическому равновесию для реакции образования малорастворимого основания назвали рН-гидратообразования.
Определим эту величину. Из уравнения для ПР следует
[OH-]=(ПР/[Меn+])1/n
Следовательно
[H+]=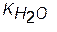 /[OH-]=
/[OH-]=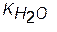 /(ПР/[Меn+])1/n
/(ПР/[Меn+])1/n
Отсюда получаем искомое выражение
ПР
pH = 14 + 1/n lg¾¾¾
[Men+]
Ваша оценка?




