Для расчета рН необходимо определить равновесное значение концентрации ионов водорода, т.е. величину [H+].
При диссоциации слабых оснований
МеОН = Ме+ + OH-
не все молекулы основания диссоциируют на ионы, а только их часть. Остальные молекулы остаются в недиссоциированном виде и находятся в равновесии с ионами гидроксила и катионами металла. В этом случае закон действующих масс принимает вид
[Me+]×[OH-]
KД = ¾¾¾¾¾
[MeOH]
где константу равновесия KД называют константой диссоциации), численное значение дается в справочнике).
Имеем одно уравнение с 3 неизвестными ([Me+],{OH-] и [MeOH]). Поэтому для нахождения неизвестных надо найти еще два недостающих уравнения.
Одно из недостающих уравнений находим таким образом. Допустим, что из-за диссоциации основания его концентрация уменьшилась на х молей. Поэтому если до диссоциации концентрация основания равнялась [MeOH]0 , то после установления равновесия она станет
[MeOH]= [MeOH]0 — х.
Второе недостающее уравнение найдем из уравнения диссоциации основания.
Из уравнения реакции следует, что из 1 моля основания образуется 1 моль ионов металла и 1 моль ионов гидроксила. Поскольку согласно схеме реакции при диссоциации основания ионы металла и гидроксила возникают в одинаковых количествах, то третьим уравнением будет условие
[Me+]×=[OH-]= x.
Следовательно, выражение для константы диссоциации принимает вид
x2
KД = ¾¾¾¾¾
[MeOH]0 — x
Отсюда можно найти концентрацию ионов водорода и рассчитать рН. Но это уравнение можно упростить, если принять, что для слабого основания реализуется условие [MeOH]0 >>x= [OH-]. В этом случае получаем
___________
x=[OH-]= ÖKД[MeOH]0
Учитывая ионное произведение воды, находим, что
___________
[H+]=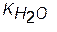 /[OH-]=
/[OH-]=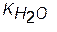 /ÖKД[MeOH]0
/ÖKД[MeOH]0
откуда, после логарифмирования, находим искомое выражение
рН= 14+1/2lg(KД) + 1/2lg([MeOH]0)
Ваша оценка?