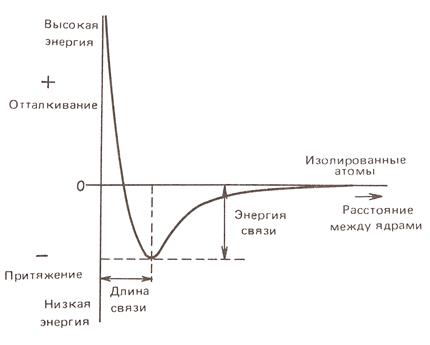
У р-элементов в некоторых случаях относительное положение s 2р- и p 2р- связывающих МО может меняться в зависимости от электрон-электронных взаимодействий между s 2s— и s 2р-молекулярными орбиталями. То же самое относится к орбиталям s* 2sи s* 2р. В результате таких взаимодействий s 2р-МО приобретают более высокую энергию, чем p 2р, а у s 2s-МО она немного снижается. Этот феномен имеет значение для образования молекул “лёгких” элементов второго периода (бор, углерод, азот); для “тяжёлых” элементов (фтор, кислород) характерно обычное расположение МО. Образование молекулы фтораЭкспериментальный факт: Стандартное состояние фтора — диамагнитный газ F2 (напомним, что частица диамагнитна, если у неё нет неспаренных электронов и парамагнитна при их наличии). Электронная конфигурация атома фтора: 1s22s22p5.Порядок заполнения молекулярных орбиталей представлен на рис. 40. Электронная формула молекулы F2 [(σ1s)2 (σ*1s)2 (σ2s)2 (σ*2s)2 (σ2рх)2 (π 2ру)2 (π2рz)2].
 |
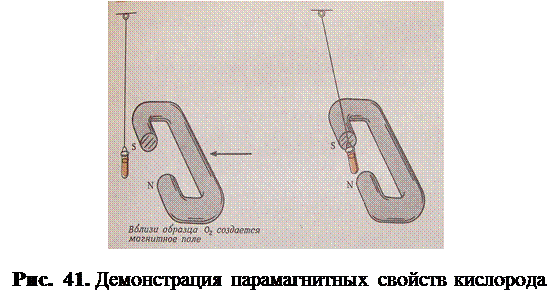
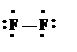 Как видно из рисунка, электроны внутреннего квантового слоя не вносят вклада в порядок связи, поэтому на молекулярной диаграмме их можно не показывать. Данный порядок связи соответствует формуле Льюиса: Образование молекулы кислородаЭкспериментальный факт: При обычных условиях кислород является газом. Молекула состоит из двух атомов, обладает парамагнитными свойствами (рис. 41), имеет два неспаренных электрона.
Как видно из рисунка, электроны внутреннего квантового слоя не вносят вклада в порядок связи, поэтому на молекулярной диаграмме их можно не показывать. Данный порядок связи соответствует формуле Льюиса: Образование молекулы кислородаЭкспериментальный факт: При обычных условиях кислород является газом. Молекула состоит из двух атомов, обладает парамагнитными свойствами (рис. 41), имеет два неспаренных электрона.
 |
Электронная конфигурация атома кислорода: 1s22s22p4. Каждый атом кислорода имеет во внешнем слое шесть валентных электронов. Эти 12 электронов должны разместиться на восьми молекулярных орбиталях (рис. 42). Электронная формула молекулы О2 [(σ1s)2 (σ*1s)2 (σ2s)2 (σ*2s)2 (σ2рх)2 (π 2ру)2 (π2рz)2 (π*2ру)1 (π*2рz)1].
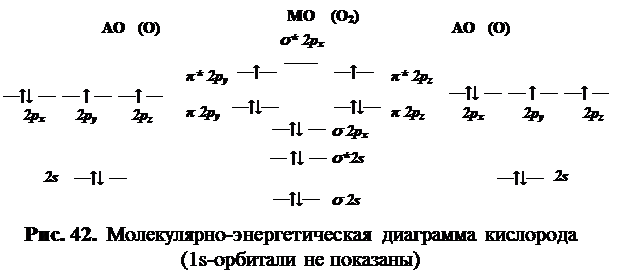 |
Четыре 2s-электрона заселяют s 2s— и s* 2s—орбитали. Два 2рx—электрона занимают s 2рх-МО, а два других — p 2р. Из оставшихся четырёх р-электронов два размещаются на связывающей p 2р-орбитали, а два (по правилу Хунда) — на двух разрыхляющих p* 2р — МО. Они имеют параллельные спины и обеспечивают молекуле кислорода парамагнитные свойства. ПС = 0,5 · (8-4) = 2.Структура Льюиса для молекулы О2 имеет вид:Согласно этой формуле, два неспаренных электрона каждого атома кислорода используются для образования двойной связи. Наличия неспаренных электронов в данной молекуле теория Льюиса не предсказывает, тогда, как метод МО даёт толкование наилучшим образом совпадающее с экспериментальными данными. Предсказание парамагнетизма молекулы кислорода является очень важным достижением метода молекулярных орбиталей. Не существует никакой другой теории химической связи, которая столь же естественным образом интерпретировала бы это свойство кислорода. Образование молекулы азотаЭкспериментальные факты: Молекула азота обладает сравнительно низкой реакционной способностью. Этот газ часто используется для создания инертной атмосферы, если исходные реагенты или продукты реакции легко взаимодействуют с кислородом воздуха или парами воды. Энергия связи в молекуле азота очень высока (945 кДж/моль), а длина связи мала (0,110 нм). Молекула азота диамагнитна.Электронная конфигурация атома азота: 1s22s22p3. Три р-электрона не спарены, для завершения октетов необходимо обобществление трёх пар электронов и образование тройной связи, кроме того у каждого атома азота остаётся одна неподелённая электронная пара. Структуры Льюиса для атомов и молекулы азота имеют вид:
ПС = 0,5 · (8-4) = 2.Структура Льюиса для молекулы О2 имеет вид:Согласно этой формуле, два неспаренных электрона каждого атома кислорода используются для образования двойной связи. Наличия неспаренных электронов в данной молекуле теория Льюиса не предсказывает, тогда, как метод МО даёт толкование наилучшим образом совпадающее с экспериментальными данными. Предсказание парамагнетизма молекулы кислорода является очень важным достижением метода молекулярных орбиталей. Не существует никакой другой теории химической связи, которая столь же естественным образом интерпретировала бы это свойство кислорода. Образование молекулы азотаЭкспериментальные факты: Молекула азота обладает сравнительно низкой реакционной способностью. Этот газ часто используется для создания инертной атмосферы, если исходные реагенты или продукты реакции легко взаимодействуют с кислородом воздуха или парами воды. Энергия связи в молекуле азота очень высока (945 кДж/моль), а длина связи мала (0,110 нм). Молекула азота диамагнитна.Электронная конфигурация атома азота: 1s22s22p3. Три р-электрона не спарены, для завершения октетов необходимо обобществление трёх пар электронов и образование тройной связи, кроме того у каждого атома азота остаётся одна неподелённая электронная пара. Структуры Льюиса для атомов и молекулы азота имеют вид:
 |
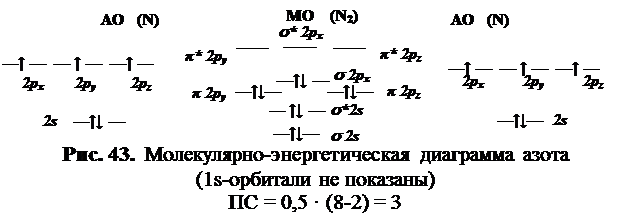
Диаграмма (рис. 43) показывает, что заполнение МО десятью валентными электронами приводит к их полному спариванию, что соответствует экспериментальным данным о диамагнетизме молекулы азота. При построении молекулярной диаграммы азота учитывается электрон-электронное взаимодействие и порядок заполнения s 2р- и p 2р- орбиталей.Такой порядок связи соответствует малому межатомному расстоянию и большой энергии связи.Для молекулы азота s—p—взаимодействия p 2р— и s 2р-орбиталей не влияют ни на порядок связи, ни на количество неспаренных электронов, однако приведённая ниже последовательность заполнения МО экспериментально подтверждается методом электронной спектроскопии.
 |
Образование молекулы углерода (С2)Экспериментальный факт: Молекула С2 диамагнитна.Электронная конфигурация основного состояния атома углерода 1s22s22p2. Структура Льюиса соответствует обобществлению четырёх электронов, образованию двойной связи, наличию у каждого атома неподелённой электронной пары; неспаренных электронов нет:
 |
Восемь валентных электронов двух атомов углерода располагаются на МО, образованных в результате комбинации 2s- и 2p-атомных орбиталей: четыре электрона занимают s 2s— и s* 2s—орбитали, а оставшиеся четыре полностью заселяют две вырожденные p 2рyz – MO. Только в этом случае молекула будет диамагнитной. Это подтверждает правильность предположения о том, что в данном случае (как и у азота) s 2рx–орбиталь имеет более высокую энергию, чем p 2рyz –орбитали. Если бы это было не так, то электронная конфигурация молекулы С2 была бы s2s2s*2s2s2рx2p2рy1p2рz1, что соответствовало бы образованию парамагнитной частицы и противоречило бы данным эксперимента. Следовательно, электронная конфигурация молекулы углерода имеет вид: s 2s2 s*2s2 p 2рy2 p 2рz2.Порядок связи в молекуле С2 = 0,5 · (6-2) = 2.
Ваша оценка?