При сближении на определённое расстояние (r1) двух атомов, содержащих электроны с антипараллельными спинами, между ними возникает сильное обменное взаимодействие: ядро первого атома начинает притягивать электрон второго и наоборот – ядро второго притягивает электрон первого. Наступает момент, когда оба электрона начинают двигаться в поле обоих ядер. С позиций квантовой механики, этот момент рассматривается как момент образования ковалентной связи. Он характеризуется наибольшей глубиной перекрывания атомных орбиталей и максимальным выделением энергии (рис. 13). Теперь электроны находятся на молекулярной орбитали. Передача одного электрона любого атома в ковалентную связь не сопровождается изменением заряда ни на одном из атомов, образующих эту связь, т.к. партнёр компенсирует эти потери.
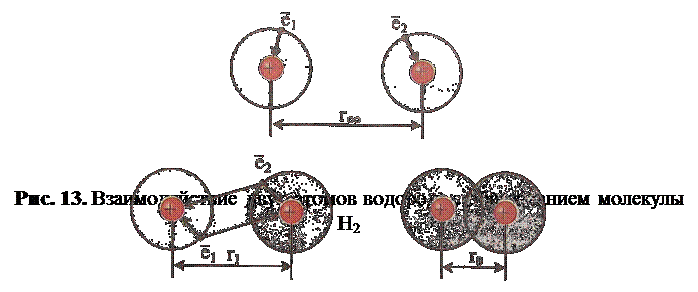 |
При сближении атомов до некоторого малого расстояния (rо) начинают играть роль силы отталкивания двух ядер, энергия системы повышается. Расстояние rо, при котором эти силы компенсируют друг друга, соответствует длине химической связи, т.е. расстоянию между атомами в молекуле, а выделившаяся энергия — энергии связи (рис. 14).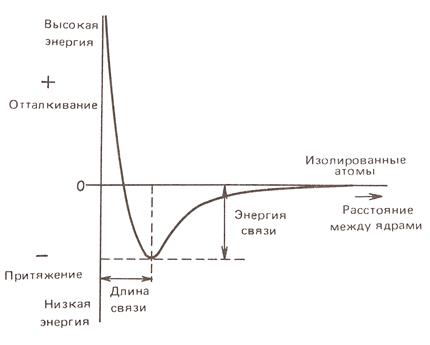
 Если взаимодействующие атомы имеют электроны с параллельными спинами, то их орбитали отталкиваются друг от друга, энергия системы возрастает, химическая связь не образуется.Впервые предположение о том, что химические связи имеют ковалентный характер и осуществляются за счёт обобщённых пар электронов было выдвинуто Г. Льюисом и В. Косселем. Льюис высказал мысль о том, что каждый атом стремится к заполнению вокруг себя устойчивой электронной оболочки инертного газа. Для атома водорода ею является двухэлектронный слой гелия, для атомов элементов второго периода — восьмиэлектронная оболочка неона. И. Лэнгмюр назвал её электронным октетом.
Если взаимодействующие атомы имеют электроны с параллельными спинами, то их орбитали отталкиваются друг от друга, энергия системы возрастает, химическая связь не образуется.Впервые предположение о том, что химические связи имеют ковалентный характер и осуществляются за счёт обобщённых пар электронов было выдвинуто Г. Льюисом и В. Косселем. Льюис высказал мысль о том, что каждый атом стремится к заполнению вокруг себя устойчивой электронной оболочки инертного газа. Для атома водорода ею является двухэлектронный слой гелия, для атомов элементов второго периода — восьмиэлектронная оболочка неона. И. Лэнгмюр назвал её электронным октетом.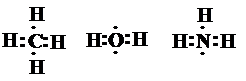 Формулы, показывающие число электронов в связях и неподелённые электронные пары на гетероатомах, назваются формулами Льюиса. В этих формулах каждая связь изображается двумя точками: В структурных формулах общая электронная пара изображается черточкой, соединяющей два атома:
Формулы, показывающие число электронов в связях и неподелённые электронные пары на гетероатомах, назваются формулами Льюиса. В этих формулах каждая связь изображается двумя точками: В структурных формулах общая электронная пара изображается черточкой, соединяющей два атома:
 |
Ваша оценка?