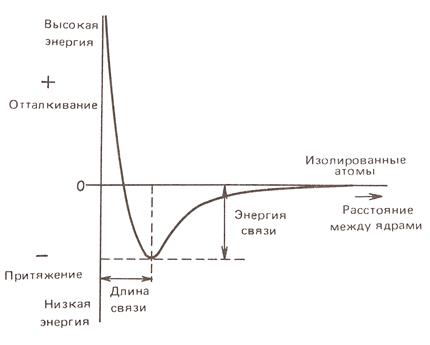
Ковалентная связь осуществляется с помощью общей электронной пары, т.е. двух электронов, которые одновременно принадлежат обоим взаимодействующим атомам. Процесс возникновения такой связи предполагает перекрывание (взаимопроникновение) атомных орбиталей. Образуется одна общая молекулярная орбиталь, при этом возрастает электронная плотность в промежутке между ядрами. Это приводит к стягиванию положительно заряженных ядер и выделению энергии, поэтому получающаяся молекула приобретает большую устойчивость, чем отдельные атомы. Подробно механизмы образования и свойства ковалентных связей будут рассмотрены в главе 3.2.2. Ионная связь
Химическая связь, которая образуется в результате электростатического взаимодействия двух разноименно заряженных ионов, возникающих при полном переносе электронов от одного атома к другому, называется ионной. Способность атомов образовывать простые ионы обусловлена их электронной структурой. Ионная связь более вероятна, если один атом обладает низкой энергией ионизации, а другой — большим сродством к электрону.
Энергия ионизации – это энергия, которую необходимо затратить, чтобы удалить один электрон из нейтрального атома, с образованием положительно заряженного иона – катиона. С увеличением атомного радиуса эта энергия уменьшается. Наименьшей энергией ионизации характеризуются элементы IА группы Периодической системы.
Na· + 120 ккал → Na+ + ē (энергия затрачивается)
Энергия сродства к электрону – это количество энергии, которое выделяется при присоединении одного электрона к нейтральному атому, с образованием отрицательно заряженного иона – аниона. Эта энергия зависит не только от атомного радиуса, но и от числа электронов во внешнем квантовом слое, а также от наличия в нём свободных атомных орбиталей. Наибольшим сродством к электрону обладают галогены.

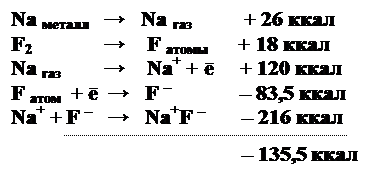 Ионная связь образуется в том случае, если взаимодействие атомов приводит к выделению энергии. Энергетический баланс образования ионной связи на примере взаимодействия атомов натрия и фтора (по Габеру – Борну):
Ионная связь образуется в том случае, если взаимодействие атомов приводит к выделению энергии. Энергетический баланс образования ионной связи на примере взаимодействия атомов натрия и фтора (по Габеру – Борну):
Выигрыш в энергии при образовании электростатически связанных ионов натрия и фтора составляет 135,5 ккал.
Выделением энергии сопровождается присоединение одного электрона. Присоединение последующих электронов, согласно квантово-механическим расчетам, невозможно. Поэтому одноатомные (простые) многозарядные ионы (например, О2-, S2-) в свободном состоянии существовать не могут. В связи с этим соединения, состоящие из простых ионов, немногочисленны. Естественно предположить, что ионная связь наиболее вероятна между атомами щелочных металлов и галогенов. Тем не менее, электронная плотность между ионами щелочных металлов и галогенов не равна нулю. Межъядерное расстояние в молекуле NaCl в газообразном состоянии равно 0,250 нм. Если бы она состояла из ионов Na+ и Cl–, то её дипольный момент должен быть равен 12Д. В действительности он равен 10Д, т.е. эффективный заряд в данном случае будет меньше 1. Подсчитано, что эффективный заряд составляет 0,8:
Na+0,8Cl –0,8.
Любую полярную связь формально можно рассматривать на n% как ионную и на (100 – n)% как ковалентную. Чем сильнее значение эффективного заряда приближается к целочисленному (1,0), тем больше связь в молекуле данного соединения приближается к ионной. Таким образом, ионная связь представляет собой крайний случай ковалентной полярной связи. В соответствии со средними значениями эффективных зарядов атомов подсчитано, что в соединении CsF связь на 93% ионная и на 7% ковалентная, в молекуле HI – на 5% ионная и на 95% ковалентная, а в молекуле HF – соответственно на 45% и 55%.
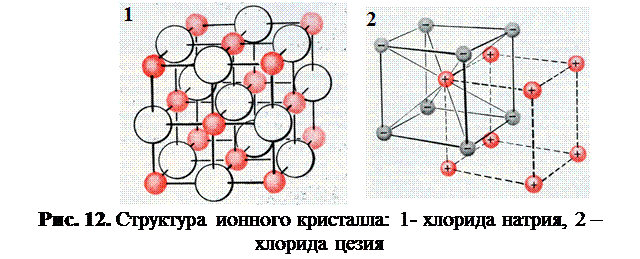
Ионная связь в отличие от ковалентной не имеет направленности и насыщаемости. Вследствие этого соединения с ионной связью в виде отдельных молекул могут существовать только в газообразном состоянии. В обычных условиях каждый катион взаимодействует со всеми анионами, находящимися поблизости в любом направлении, и наоборот. Это сопровождается формированием ассоциаций — ионных кристаллов типа (Na+Cl–)х (рис.12). Применение к ним понятия «молекула» условно, оно показывает количественное соотношение ионов в соединении. В водных растворах такие вещества легко диссоциируют на ионы, которые сразу гидратируются, образуя новые ассоциации – гидраты.
 |
Ваша оценка?