ПЕРВЫЙ ПЕРИОД Водород Водород является элементом первого периода. Его атом имеет только один квантовый слой, который содержит одну орбиталь — 1s. На этой орбитали находится один электрон. Электронная конфигурация атома водорода — 1s1.
|
Символ Льюиса: Электронная диаграмма: 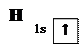 Единственный электрон атома водорода может принимать участие в образовании только одной химической связи с другими атомами:
Единственный электрон атома водорода может принимать участие в образовании только одной химической связи с другими атомами: 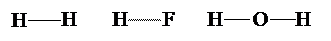 Количество ковалентных связей, которые образует атом в данном соединении, характеризует его валентность. Во всех соединениях атом водорода одновалентен. ГелийГелий, как и водород, — элемент первого периода. В своём единственном квантовом слое он имеет одну s-орбиталь, на которой находится два электрона с антипараллельными спинами (неподелённая электронная пара). Символ Льюиса: Не: . Электронная конфигурация 1s2, её графическое изображение:
Количество ковалентных связей, которые образует атом в данном соединении, характеризует его валентность. Во всех соединениях атом водорода одновалентен. ГелийГелий, как и водород, — элемент первого периода. В своём единственном квантовом слое он имеет одну s-орбиталь, на которой находится два электрона с антипараллельными спинами (неподелённая электронная пара). Символ Льюиса: Не: . Электронная конфигурация 1s2, её графическое изображение: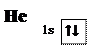 В атоме гелия нет неспаренных электронов, нет свободных орбиталей. Его энергетический уровень является завершённым. Атомы с завершённым квантовым слоем не могут образовывать химических связей с другими атомами. Они называются благородными или инертными газами. Гелий — их первый представитель. ВТОРОЙ ПЕРИОД ЛитийАтомы всех элементов второго периода имеют два энергетических уровня. Внутренний квантовый слой — это завершённый энергетический уровень атома гелия. Как было показано выше, его конфигурация выглядит как 1s2, но для её изображения может быть также использована и сокращённая запись: [He]. В некоторых литературных источниках её обозначают [К] (по наименованию первой электронной оболочки).Второй квантовый слой лития содержит четыре орбитали (22 = 4): одну s и три р. Электронная конфигурация атома лития: 1s22s1 или [He] 2s1. C помощью последней записи выделяются только электроны внешнего квантового слоя (валентные электроны). Символ Льюиса для лития — •Li. Графическое изображение электронной конфигурации:
В атоме гелия нет неспаренных электронов, нет свободных орбиталей. Его энергетический уровень является завершённым. Атомы с завершённым квантовым слоем не могут образовывать химических связей с другими атомами. Они называются благородными или инертными газами. Гелий — их первый представитель. ВТОРОЙ ПЕРИОД ЛитийАтомы всех элементов второго периода имеют два энергетических уровня. Внутренний квантовый слой — это завершённый энергетический уровень атома гелия. Как было показано выше, его конфигурация выглядит как 1s2, но для её изображения может быть также использована и сокращённая запись: [He]. В некоторых литературных источниках её обозначают [К] (по наименованию первой электронной оболочки).Второй квантовый слой лития содержит четыре орбитали (22 = 4): одну s и три р. Электронная конфигурация атома лития: 1s22s1 или [He] 2s1. C помощью последней записи выделяются только электроны внешнего квантового слоя (валентные электроны). Символ Льюиса для лития — •Li. Графическое изображение электронной конфигурации:
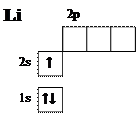 |
Поскольку завершённый внутренний энергетический уровень не принимает участия в образовании химических связей, то в дальнейшем в электронных диаграммах мы будем изображать только конфигурацию внешнего квантового слоя. Атом лития во внешнем электронном уровне имеет один неспаренный электрон, следовательно он может образовать одну химическую связь с атомами других элементов:
|
БериллийЭлектронная конфигурация — [He] 2s2. Электронная диаграмма внешнего квантового слоя:
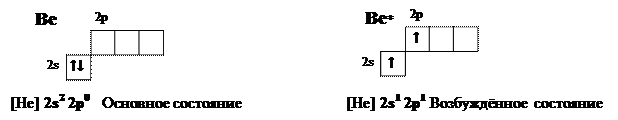 |
Атом бериллия способен переходить в возбуждённое состояние: за счет потребления некоторого количества энергии один из s-электронов меняет спин и переходит на свободную р-орбиталь. Энергетические затраты на возбуждение компенсируются при образовании химических связей. Возбуждённый атом бериллия имеет два неспаренных электрона (• Ве•) и может образовать две химических связи с другими атомами:
|
БорЭлектронная конфигурация — [He] 2s22р1. Атом бора может переходить в возбуждённое состояние. Электронная диаграмма внешнего квантового слоя:
В возбуждённом состоянии атом бора имеет три неспаренных электрона и может образовать три химических связи: ВF3, B2O3.При этом у атома бора остаётся свободная орбиталь, которая может участвовать в образовании связи по донорно-акцепторному механизму. Углерод Электронная конфигурация — [He] 2s22р2. Электронные диаграммы внешнего квантового слоя атома углерода в основном и возбуждённом состояниях:

Невозбуждённый атом углерода может образовать две ковалентных связи за счёт спаривания электронов и одну — по донорно-акцепторному механизму. Примером такого соединения является оксид углерода (II), который имеет формулу СО и называется угарным газом. Подробнее его строение будет рассмотрено в разделе 2.1.2. Возбуждённый атом углерода уникален: все орбитали его внешнего квантового слоя заполнены неспаренными электронами, т.е. число валентных орбиталей и валентных электронов у него одинаково. Идеальным партнёром для него является атом водорода, у которого на единственной орбитали находится один электрон. Этим объясняется их способность к образованию углеводородов. Имея четыре неспаренных электрона, атом углерода образует четыре химических связи: СН4, СF4, СО2.В молекулах органических соединений атом углерода всегда находится в возбуждённом состоянии:
|
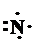 Азот Электронная конфигурация — [He] 2s22р3. Символ Льюиса: Электронная диаграмма внешнего квантового слоя:
Азот Электронная конфигурация — [He] 2s22р3. Символ Льюиса: Электронная диаграмма внешнего квантового слоя:
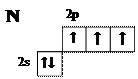 |
Атом азота не может возбуждаться, т.к. в его внешнем квантовом слое нет свободной орбитали. Он образует три ковалентных связи за счёт спаривания электронов:
|
Неподелённая электронная пара азота может участвовать в образовании связи по донорно-акцепторному механизму. 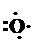 КислородЭлектронная конфигурация — [He] 2s22р4. Символ Льюиса: Электронная диаграмма внешнего квантового слоя:
КислородЭлектронная конфигурация — [He] 2s22р4. Символ Льюиса: Электронная диаграмма внешнего квантового слоя:
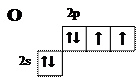 |
Имея два неспаренных электрона во внешем слое, атом кислорода образует две ковалентных связи:
|
Кроме того, за счёт неподелённой электронной пары атом кислорода может образовать связь по донорно-акцепторному механизму. 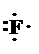 ФторЭлектронная конфигурация — [He] 2s22р5. Символ Льюиса: Электронная диаграмма внешнего квантового слоя:
ФторЭлектронная конфигурация — [He] 2s22р5. Символ Льюиса: Электронная диаграмма внешнего квантового слоя: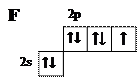 За счёт неспаренного электрона атом фтора может образовать одну ковалентную связь:
За счёт неспаренного электрона атом фтора может образовать одну ковалентную связь:
|
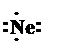 НеонЭлектронная конфигурация — [He] 2s22р6. Символ Льюиса: Электронная диаграмма внешнего квантового слоя:
НеонЭлектронная конфигурация — [He] 2s22р6. Символ Льюиса: Электронная диаграмма внешнего квантового слоя:
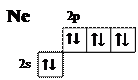 |
Атом неона имеет завершённый внешний энергетический уровень и не образует химических связей ни с какими атомами. Это второй благородный газ. ТРЕТИЙ ПЕРИОД Атомы всех элементов третьего периода имеют три квантовых слоя. Электронную конфигурацию двух внутренних энергетических уровней можно изображать как [Ne]. Внешний электронный слой содержит девять орбиталей, которые заселяются электронами, подчиняясь общим закономерностям. Так, для атома натрия электронная конфигурация имеет вид: [Ne] 3s1, для кальция — [Ne] 3s2 (в возбуждённом состоянии — [Ne] 3s13р1), для алюминия — [Ne] 3s23р1 (в возбуждённом состоянии — [Ne] 3s13р2). В отличие от элементов второго периода, атомы элементов V – VII групп третьего периода могут существовать как в основном, так и в возбуждённом состояниях.ФосфорФосфор является элементом пятой группы. Его электронная конфигурация — [Ne] 3s23р3. Подобно азоту, он имеет три неспаренных электрона на внешнем энергетическом уровне и образует три ковалентных связи. Примером является фосфин, имеющий формулу РН3 (сравните с аммиаком). Но фосфор, в отличие от азота, во внешнем квантовом слое содержит свободные d-орбитали и может переходить в возбуждённое состояние — [Ne] 3s13р3d1:
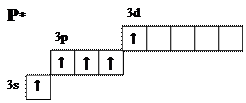 Это даёт ему возможность образовать пять ковалентных связей в таких, например, соединениях как Р2О5 и Н3РО4.
Это даёт ему возможность образовать пять ковалентных связей в таких, например, соединениях как Р2О5 и Н3РО4.
СераЭлектронная конфигурация основного состояния — [Ne] 3s23p4. Электронная диаграмма:
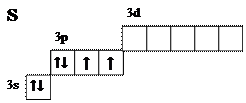 |
В основном состоянии атом серы образует только две химических связи:
|
Однако он может возбуждаться, переводя электрон вначале с р— на d-орбиталь (первое возбуждённое состояние), а затем с s— на d-орбиталь (второе возбуждённое состояние):
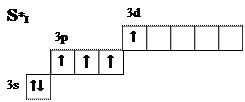 |
В первом возбуждённом состоянии атом серы образует четыре химических связи в таких соединениях как SО2 и H2SO3. Второе возбуждённое состояние атома серы можно изобразить с помощью электронной диаграммы:
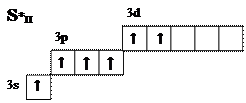 |
Такой атом серы образует шесть химических связей в соединениях SO3 и H2SO4.
1.3.3. Электронные конфигурации атомов элементов больших периодов ЧЕТВЁРТЫЙ ПЕРИОД
Начинается период с калия (19K) электронная конфигурация: 1s22s22p63s23p64s1 или [Ar] 4s1 и кальция (20Ca): 1s22s22p63s23p64s2 или [Ar] 4s2. Таким образом, в соответствии с правилом Клечковского, после р-орбиталей Ar заполняется внешний 4s-подуровнь, который обладает меньшей энергией, т.к. 4s-орбиталь проникает ближе к ядру; 3d-подуровень остается незаполненным (3d0). Начиная от скандия, у 10 элементов происходит заселение орбиталей 3d-подуровня. Они называются d-элементами.
|
В соответствии с принципом последовательного заполнения орбиталей, у атома хрома электронная конфигурация должна быть [Ar] 4s23d4, однако у него наблюдается «проскок» электрона, заключающийся в переходе 4s-элекрона на близкую по энергии 3d-орбиталь (рис. 11).
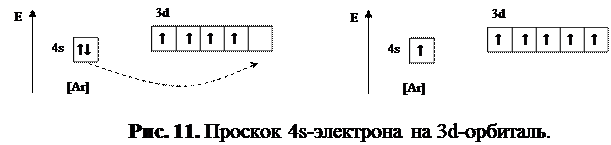 |
Экспериментально установлено, что состояния атома, при которых p-, d-, f-орбитали заполнены наполовину (p3, d5, f7), полностью (p6, d10, f14) или свободны (p0, d0, f0), обладают повышенной устойчивостью. Поэтому если атому до полузавершения или завершения подуровня не хватает одного электрона, наблюдается его «проскок» с ранее заполненной орбитали (в данном случае — 4s).
За исключением Cr и Cu, все элементы от Ca до Zn имеют одинаковое количество электронов на внешнем уровне – два. Этим объясняется относительно небольшое изменение свойств в ряду переходных металов. Тем не менее, для перечисленных элементов валентными являются как 4s-электроны внешнего, так и 3d-электроны предвнешнего подуровня (за исключением атома цинка, у которого третий энергетический уровень полностью завершён).
Далее следует заполнение электронами 4p-орбиталей. Данный процесс ничем не нарушается и соответствует построению типических элементов от галлия (Ga) до инертного газа криптона Kr (p-элементы):
|
Свободными остались 4d и 4f орбитали, хотя четвертый период завершен.
ПЯТЫЙ ПЕРИОД
Последовательность заполнения орбиталей та же, что и в предыдущем периоде: сначала заполняется 5s-орбиталь (37Rb [Kr] 5s1), затем 4d и 5p (54Xe [Kr] 5s24d105p6). Орбитали 5s и 4d ещё более близки по энергии, поэтому у большинства 4d-элементов (Mo, Tc, Ru, Rh, Pd, Ag) наблюдается переход электрона с 5s на 4d-подуровень.
ШЕСТОЙ И СЕДЬМОЙ ПЕРИОДЫ
В отличие от предыдущего шестой период включает 32 элемента. Цезий и барий – это 6s-элементы. Следующие энергетически выгодные состояния это 6p, 4f и 5d. Вопреки правилу Клечковского, у лантана заполняется не 4f а 5d-орбиталь (57La [Xe] 6s25d1), однако у следующих за ним элементов происходит заполнение 4f-подуровня (58Ce [Xe] 6s24f2), на котором четырнадцать возможных электронных состояний. Атомы от церия (Се) до лютеция (Lu) называются лантаноидами – это f-элементы. В ряду лантаноидов, иногда происходит «проскок» электрона, так же как в ряду d-элементов. Когда 4f-подуровень оказывается завершенным, продолжает заполняться 5d-подуровень (девять элементов) и завершают шестой период, как и любой другой, кроме первого, шесть р-элементов.
Первые два s-элемента в седьмом периоде – это франций и радий, за ними следует один 6d-элемент – актиний (89Ac [Rn] 7s26d1). За актинием следует четырнадцать 5f-элементов – актиноидов. За актиноидами должны следовать девять 6d-элементов и завершать период должны шесть р-элементов. Седьмой период является незавершенным.
Рассмотренная закономерность формирования периодов системы элементами и заполнения атомных орбиталей электронами показывает периодическую зависимость электронных структур атомов от заряда ядра.
Период – это совокупность элементов, расположенных в порядке возрастания зарядов ядер атомов и характеризующихся одинаковым значением главного квантового числа внешних электронов. В начале периода заполняются ns-, а в конце – np-орбитали (кроме первого периода). Эти элементы образуют восемь главных (А) подгрупп периодической системы Д.И. Менделеева.
Главная подгруппа – это совокупность химических элементов, расположенных по вертикали и имеющих одинаковое число электронов на внешнем энергетическом уровне.
В пределах периода с увеличением заряда ядра и возрастающей силы притяжения к нему внешних электронов слева направо уменьшаются радиусы атомов, что в свою очередь обусловливает ослабление металлических и возрастание неметаллических свойств. За атомный радиус принимают теоретически рассчитанное расстояние от ядра до максимума электронной плотности внешнего квантового слоя. В группах сверху вниз увеличивается число энергетических уровней, а, следовательно, и атомный радиус. При этом металлические свойства усиливаются. К важным свойствам атомов, которые изменяются периодически в зависимости от зарядов ядер атомов, также относятся энергия ионизации и сродство к электрону, которые будут рассмотрены в разделе 2.2.
Ваша оценка?