Важнейшие свойства металлов тесно связаны со строением их кристаллических решеток. У металлов встречаются структуры трех следующих типов: гранецентрированная кубическая (ГЦК), гексагональная (Г), объемноцентрированная кубическая (ОЦК).
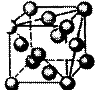
а б в
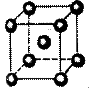
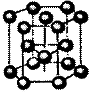
Рис. 4. Виды основных кристаллических решеток металлов:
а – объемноцентрированная кубическая;
б – гранецентрированная кубическая;
в – гексагональная
Объемноцентрированная кубическая решетка имеется в металлах: Li, Na, K, V, Cr, Fe при температурах до 911° и от 139° до плавления у Pb, W и др.; гранецентрированная кубическая – Al, Ca, Fe при температурах от 911 до 1 392 °С, Ni, Cu, Ag, Au и др. Гексагональная характерна для Be, Mg, Cd, Co, Zn и др.
Атомы металлов в металлическом кристалле образуют плотноупакованные структуры, где не обнаруживается никакой видимой связи с их валентностью. Удерживаются атомы в едином кристалле за счет металлической связи. Кристаллическая решетка металла состоит из его ионов и подвижных электронов. Взаимодействие ионов решетки с «электронной решеткой» и обеспечивает прочность кристалла.
При образовании ОЦК решетки, которая свойственна, например, металлическому натрию, атом, имея один валентный электрон образует металлическую связь с другими атомами. В то же время остальные его валентные орбитали являются вакантными. Избыток числа орбиталей над числом электронов приводит к образованию такой структуры, когда каждый атом натрия «создает» у себя устойчивую восьми – электронную оболочку благородных газов. Это достигается при количестве ближайших атомов (координационном числе), равном восьми. Аналогично атом хрома в основном состоянии имеет электронную конфигурацию Cr …3s2p6d54s1 с одним валентным s-электроном, как у натрия. Его кристаллическая решетка также является решеткой ОЦК.
Всегда по известной конфигурации атома можно определить симметрию кристаллической решетки простого вещества данного элемента. Так, алюминию с электронной конфигурацией атома в возбужденном состоянии Al* …3s1p2 свойственно ГЦК решетка (К.Ч. = 12), а для атомов магния (Mg* …3s1p1), скандия (Sc* …4s1p1) – гексагональная решетка.
d-элементов их
(n – 1) d— электроны практически не влияют. Но если атом металла содержит неспаренные d-электроны, то эти электроны могут
взаимодействовать с d-электронами соседних атомов металла и образовывать дополнительные ковалентные связи. Аналогичное взаимодействие возможно и для p-элементов. В этих металлах существуют металлическая и ковалентная связи одновременно. Ковалентная локализованная связь обладает свойством направленности, а металлическая – ненаправленная связь. Поэтому первый вид связи обуславливает более упорядоченное состояние, а второй – менее упорядоченное, т. е. характеризуется большей энтропией. При более высоких температурах на структуре кристаллической решетки и свойствах простого вещества сказывается, в основном, наличие металлической связи. Понижение температуры приводит к уменьшению отрицательного энтропийного (– Т × ΔS) вклада в изменение энергии Гиббса и начинает преобладать более упорядоченная локализованная ковалентная связь. Типичным примером проявления этого эффекта является олово. Так, стабильной модификацией олова при t > 13,2 °C является мягкий металл – «белое» олово, в то время как при более низких температурах – устойчивее «серое» олово, представляющее собой твердый и хрупкий порошок с кристаллической решеткой типа алмаза – кристалла с ковалентной связью.
Ваша оценка?



