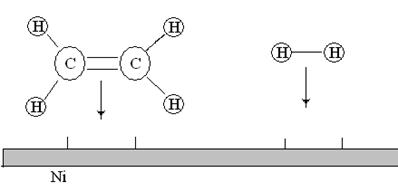
Скорость химических реакций сильно зависит от температуры. Согласно эмпирическому правилу Вант-Гоффа (1884) при повышении температуры на 10 градусов скорость большинства реакций возрастает в 2—4 раза. Число, показывающее, во сколько раз возрастает скорость реакции при повышении температуры на 10 градусов, называется температурным коэффициентом (γ) скорости данной реакции.
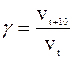
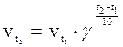
Однако, расчеты, выполненные в соответствии с молекулярно-кинетической теорией газов и жидкостей показывают, что число столкновений реагирующих молекул очень велико и нагрев на 100С увеличивает его незначительно. Если бы каждое соударение завершалось химическим взаимодействием, то практически все реакции заканчивались бы мгновенно, подобно взрыву. Однако этого не происходит. Значит не любое столкновение молекул реагирующих веществ приводит к образованию продуктов реакции.
Шведский химик Сванте Аррениус в 1889 высказал мысль, что в реакцию вступают лишь те столкнувшиеся молекулы, у которых кинетическая энергия превышает некоторую минимальную величину, характерную для данной реакции, называемую энергией активации. Такие молекулы получили называние активных.
Молекулы обладают разной кинетической энергией и, следовательно, неодинаковой скоростью движения. Используя специальные методы математической статистики и теории вероятности, для каждой температуры можно получить количественное описание этого распределения (Максвелла).
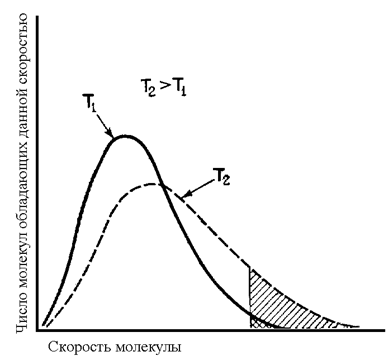
Рис. 3. Распределение молекул кислорода по скоростям при разных температурах
Максимумы на кривых отвечают наиболее вероятной скорости при указанной температуре.
Например: при 20°С около 10% молекул кислорода обладают скоростями, превышающими 700 м/с. А при 100 градусов доля молекул со скоростями, превышающими 700 м/с, становится равной 17 %.
Та дополнительная энергия, которую надо придать молекулам реагирующих веществ для того, чтобы сделать их активными, называется энергией активации Еа. Она определяется природой реагирующих веществ и служит важной кинетической характеристикой любой химической реакции.
Уравнение Аррениуса связывает константу скорости реакции с ее энергией активации:
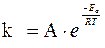
где: k — константа скорости реакции;
A —предэкспоненциальный множитель (множитель Аррениуса), постоянный для данной реакции;
e— основание натурального логарифма;
Ea- энергия активации, Дж/моль;
Т – температура, K;
R – универсальная газовая постоянная, 8,314 Дж/моль K.
Из приведенного уравнения очевидно, что чем выше энергия активации, тем меньше будет константа скорости реакции. Поэтому реакции с очень малыми значениями Еа (меньше 40 кДж/моль), протекают практически мгновенно. Если Еа очень велика (превышает 120 кДж/моль), например, в случае окисления молекулярного азота или диоксида серы кислородом, то ход реакции при обычных температурах заметить невозможно.
Важным фактором, оказывающим влияние на скорость химических реакций, является природа образующихся промежуточных продуктов, которые в химической кинетике именуются активированными комплексами или переходными состояниями. На их образование как раз и необходима энергия активации.
Рассмотрим их на примере взаимодействия в газовой фазе иода и водорода с образованием иодоводорода:
H2 + I2 → 2 HI+ 15,9 кДж
В ходе химического превращения система из исходного энергетического состояния (с суммарной энтальпией всех компонентов ΣHисх.) переходит в конечное состояние (с суммарной энтальпией ΣHпрод.) с изменением энтальпии ΔH = -15,9 кДж.
Взаимодействуют только молекулы, которые имеют энергию, равную или превышающую энергию активации. При сближении активных молекул H2 и I2 возникает промежуточное состояние — активированный комплекс определенной конфигурации:
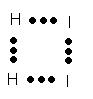 |
Рис.4. Конфигурация активированного комплекса
В активированном комплексе молекулы исходных веществ еще не совсем исчезли, а молекулы продуктов реакции не совсем образовались. Поэтому по сути своей он является переходным, неустойчивым и существует очень короткое время. Он быстро распадается с образованием конечного продукта реакции HI.
Расчеты показывают, что протекание реакции через образование активированного комплекса требует меньшей энергии активации, чем через возникновение новых связей после полной диссоциации молекул исходных веществ. Экспериментально найденная энергия активации рассматриваемой реакции (170,5 кДж/моль) оказывается намного меньше, чем энергия полного разрыва связей в молекулах иода и водорода (580,5 кДж/моль). Поэтому большинство химических реакций проходит через формирование активированных комплексов. С образованием активных комплексов связано явление катализа.
Ваша оценка?