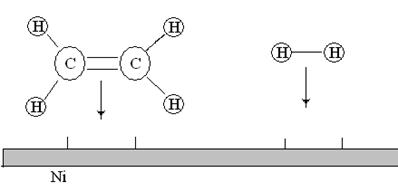
Любая гетерогенная реакция имеет, по меньшей мере, три последовательные стадии:
1. Подвод реагирующего вещества к поверхности раздела фаз;
2. Химическое взаимодействие на поверхности раздела фаз;
3. Отвод продуктов реакции от поверхности.
Скорость гетерогенной реакции определяется скоростью наименее быстрой ее стадии.
Часто самыми медленными стадиями реакции оказываются подвод реагирующего вещества к поверхности раздела фаз или отвод продуктов реакции. В этом случае скорость реакции определяется скоростью переноса веществ. Например, при растворении мрамора в соляной кислоте скорость химической стадии реакции очень велика и потому скорость реакции в целом лимитируется скоростью подвода и отвода веществ от реакционной поверхности. Именно поэтому скорость реакции сильно возрастает при измельчении мрамора, поскольку при этом увеличивается поверхность раздела фаз.
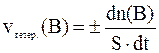
Однако есть реакции, где самой медленной стадией является химическое взаимодействие. Например, окисление железа кислородом влажного воздуха. В этом случае при увеличении скорости подвода воздуха скорость реакции в целом не изменяется.
В том случае, когда лимитирующей стадией гетерогенной реакции является химическое взаимодействие, в кинетическом уравнении учитываются концентрации только тех исходных веществ, которые находятся в газовой фазе или в растворе. Концентрации твердых веществ не включаются в кинетическое уравнение.
Например, для процесса разрушения известняка диоксидом серы, содержащимся в виде примеси в атмосферном воздухе:
СаСО3 +S02 =CaSO3 +СО2
Закон действующих масс выразится уравнением
v = k·c(SO2 )
Т.е. скорость реакции пропорциональна только концентрации диоксида серы.
Для выражения скорости гетерогенных процессов, в которых самой медленной стадией является перенос реагирующих веществ и продуктов реакции используются кинетические уравнения, учитывающие специфику процесса. Например, Уравнение Яндера для случая взаимодействия твердых веществ содержит такие величины, как начальный радиус зерен реагирующих веществ и коэффициенты диффузии веществ.
Ваша оценка?