Физические свойства металлов. Как было показано в гл. 4, находящиеся в металлической решетке ионы связаны друг с другом не-локализованными подвижными электронами. Разность энергии молекулярных орбиталей в зоне проводимости металла невелика, поэтому электроны, возбуждаясь, относительно легко переходят из одной ор-битали в другую. Этим объясняется высокие электрическая проводимость и теплопроводность металлов. Максимальную электрическую проводимость имеют серебро, медь, золото и алюминий. Ионы металлов в кристалле могут скользить относительно друг друга. Этим объясняется ковкость (способность к расплющиванию) и пластичность (способность вытягиваться в проволоку и ленту). Плотность металлов, как и других простых веществ находится в периодической зависимости от порядкового номера элемента (рис. 11.2).
p, г/см3
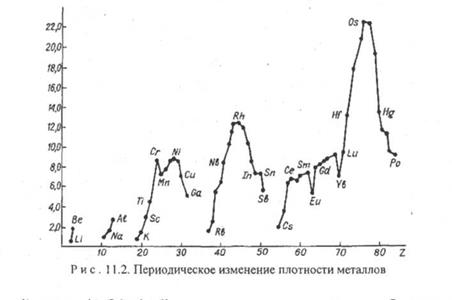
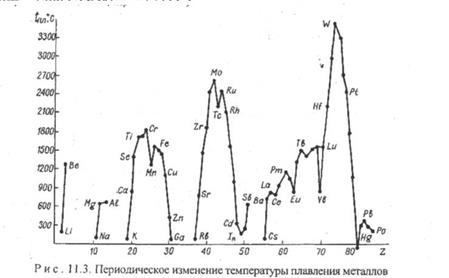
К легким (р £ 5 г/см3) относятся s-металлы и алюминий, скандий и титан, минимальную плотность имеет литий (р = 0,53 г/см» ), к тяжелым относятся в основном d-металлы 5-7 периодов. Максимальную плотность имеет осмий (р = 22,6 г/см3). Температура плавления металлов также имеет периодическую зависимость от порядкового номера элемента (рис. 11.3). К легкоплавким относятся в основном s-и р-металлы, а также d-металлы II группы. К тугоплавким (tпл выше 1500 С) принадлежат, в основном, d-металлы IV — VIII групп. Минимальную температуру плавления имеет ртуть (tпл = — 33,6 °С), максимальную — вольфрам (tпя = 3380 °С).
|
|
Физико-химические свойства металлов. Вследствие ненасыщенности и ненаправленности металлической связи для кристаллических решеток металлов характерна высокая плотность упаковки. Большинство металлов кристаллизуется с образованием гексагональных или кубических (гранецентрированных или объемно центрированных) решеток. Так как разница энергий решеток металлов относительно невелика, то большинство металлов полиморфны. Например, железо имеет четыре модификации: α(tпер = 769°С), β(tпер= 910°С), γ (tпер = 1400°С) и δ( tпер =1539°C).
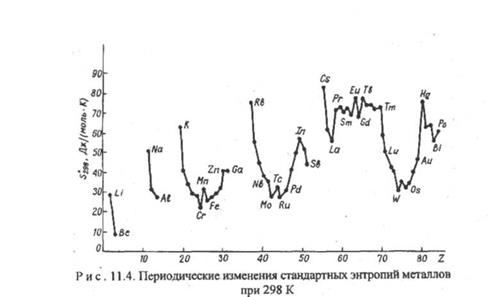
Как известно, о степени неупорядоченности можно судить по энтропии. Энтропия металлов находится в периодической зависимости от порядкового номера элемента (рис. 11.4), причем эта зависимость в значительной степени обратна ходу кривых температура плавления — порядковый номер элемента (см. рис. 11.3). Высокую энтропию имеют калий, цезий, рубидий,f-элементы, жидкая ртуть. Минимальная энтропия [ниже 30 Дж/(моль×К)] у бериллия, алюминия, хрома, железа, молибдена, рутения, вольфрама и осмия.
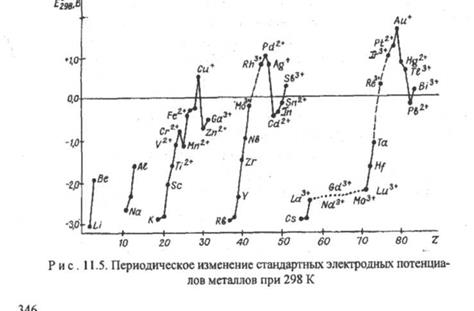
Все металлы — восстановители. О восстановительных способностях металлов судят по электродным потенциалам, значения которых также являются периодической функцией порядкового номера элемента. Так как потенциалы зависят не только от природы металлов и раствора, но и от степени окисления его ионов, то сравнение потенциалов необходимо проводить либо при одинаковой, либо при максимальной степени окисления. Однако, пока это невозможно из-за
отсутствия всех термодинамических данных. Поэтому приведенные на рис. 11.5 стандартные потенциалы относятся к ионам со степенью окисления либо равной номеру группы, либо указанной на графике. Как видно, к наиболее сильным восстановителям относятся щелочные и щелочноземельные металлы, бериллий, магний, алюминий, лантаноиды и d-металлы Ш и IV групп. Наиболее положительные электродные потенциалы имеют d-металлы I группы и платиновые металлы.
Химические свойства металлов. Будучи восстановителями, металлы могут взаимодействовать с окислителями. Термодинамическая возможность реакции металла с тем или иным окислителем определяется условием DG < 0 или Еок/в > ЕМn+/М, где Еок/в и ЕМn+/М — потенциалы окислителя и металла. Сравнение ряда потенциалов окислителей
F2/F- С12/Сl- Вг2/Вг- О2/ОН- Н2О,Н+ /Н2
+2,87 +1,36 +1,07 +1,23 (рН 0) 0,0 (рН 0)
+0,80 (рН 7) -0,42 (рН 7)
с электродными потенциалами металлов (рис. 11.5) приводит к следующим выводам. Все металлы окисляются фтором и могут окисляться хлором. Большинство металлов (кроме платины и золота) могут окисляться бромом и кислородом в кислой среде. В нейтральной среде кислород не может окислять золото, платиновые металлы, ртуть, серебро. Ионы водорода в кислой среде могут окислять многие металлы, кроме платиновых, ртути, золота, серебра, меди, рения, сурьмы и висмута. Однако, реальная возможность окисления того или иного металла определяется не только термодинамикой, но и кинетикой процесса. Взаимодействие многих металлов с хлором, бромом, кислородом, ионами водорода и другими окислителями тормозится

 пассивными пленками на поверхности металлов. Большой склонностью к пассивации обладают бериллий, алюминий, d-металлы IV—VIII групп. Многие металлы катализируют различные химические и электрохимические реакции. На рис. 11.6 приведены значения логарифмов плотностей тока обмена (константы скорости реакции) выделения водорода в кислых растворах. Как видно, наблюдается периодическая зависимость константы скорости реакции от порядкового номера элемента, максимальная скорость реакции наблюдается на d-металлах VIII группы. Высокую каталитическую активность проявляют эти металлы и в других реакциях.
пассивными пленками на поверхности металлов. Большой склонностью к пассивации обладают бериллий, алюминий, d-металлы IV—VIII групп. Многие металлы катализируют различные химические и электрохимические реакции. На рис. 11.6 приведены значения логарифмов плотностей тока обмена (константы скорости реакции) выделения водорода в кислых растворах. Как видно, наблюдается периодическая зависимость константы скорости реакции от порядкового номера элемента, максимальная скорость реакции наблюдается на d-металлах VIII группы. Высокую каталитическую активность проявляют эти металлы и в других реакциях.
Пыль и пары некоторых металлов токсичны. Как известно, токсичность характеризуется предельно-допустимыми концентрациями веществ в рабочей зоне, ПДК (мг/м3). К наиболее токсичным относятся металлы (ПДК — мг/м3): Be (10 -3), Hg (103), Pb (10-3), Cd (10 -2), Ag(10-2),Ni, Rh, Tl, In(10-1).
Так как металлы и их катионы имеют вакантные молекулярные орбитали, то большинство из них являются комплексообразователями и соответственно входят в состав комплексных соединений (см. §3.3). Способность к комплексообразованию растет с увеличением заряда иона и уменьшением его радиуса, зависит от природы металла и наличия вакантных орбиталей у его ионов. Наиболее выражена склонность к комплексообразованию у ионов переходных металлов, особенно d- элементов VIII, I и П группы. Комплексные соединения, особенно железа, кобальта, меди, марганца, хрома, ванадия, цинка и молибдена, входят в состав биологических систем, включая ферменты, переносчики крови и т.д. Например, в гемоглобин крови входит комплексное соединение железа.
Итак, химические свойства металлов находятся в периодической зависимости от их порядковых номеров.
Вопросы для самоконтроля
11.4. Почему s- металлы имеют низкие значения плотностей и температур плавления?
U.S. Почему при опускании стальных образцов в раствор, содержащий ионы меди, на образцах осаждается медь?
11.6. Какие металлы могут и какие не могут вытеснять ионы водорода из раствора с рН О?
Возможно ли самопроизвольное окисление меди и висмута ионами водоро-
да и бромом при рН 0 и рН 7?
Какое число лигандов могут координировать ионы Zn2+ и Pt4*?
Ваша оценка?