Электролизом называют процессы, происходящие на электродах под действием электрического тока, подаваемого от внешнего источника. При электролизе происходит превращение электрической энергии в химическую. Ячейка для электролиза, называемая электролизером, состоит из двух электродов и электролита. Электрод, на котором идет реакция восстановления (катод), у электролизера подключен к отрицательному полюсу внешнего источника тока. Электрод, на котором протекает реакция окисления (анод), подключен к положительному полюсу источника тока.
При электролизе можно проводить реакции, самопроизвольное протекание которых невозможно согласно термодинамическим законам. Например:
ситнез
Н2 (г) + С12 (г) + Н2О «2 НС1 (р-р);
электролиз
DrG0 = -131 кДж.
В данном случае на катоде восстанавливаются (разряжаются) ионы водорода:
2Н+ + 2е ® Н20, а на аноде идет окисление ионов хлора:
2Сl—2е ® С120.
Последовательность восстановления ионов на катоде зависит:
— от концентрации ионов в растворе, чем больше концентрация ионов, тем легче они восстанавливаются;
— активности металла, т. е. от величины стандартного электродного потенциала (j0), чем больше j0, тем менее активный металл, тем легче его ионы восстанавливаются.
Электрохимический ряд напряжения по восстановительной способности ионов металла можно разделить на три группы:
1) катионы металлов от Li+ до А13+ включительно не восстанавливаются, а вместо них восстанавливаются молекулы воды:
2Н2О + 2е = Н2 + 2ОН- (рН ³ 7)
или
2H+ + 2е = Н2 (рН < 7).
Металлы могут быть получены электролизом их расплавленных солей, в которых ионы Н+ отсутствуют;
2) катионы металлов от Мп2+ до Н+ при электролизе восстанавливаются одновременно с водородом из-за явления перенапряжения:
Zn2 + 2е = Zn0,
2Н2О + 2е = Н2 + 2ОН- (рН>7),
2H+ + 2е = Н20 (pH<7);
3) катионы металлов от Сu + до Аu3+ практически полностью восстанавливаются без восстановления водорода:
Сu2+ + 2е = Сu0.
Последовательность разрядки ионов на аноде зависит как от природы аниона, так и от вещества, из которого сделан анод. Различают нерастворимые (инертные) аноды и растворимые (активные). К первым относят электроды из угля, графита, платины, ко вторым — из металлов.
На инертных анодах окисляются в первую очередь элементарные ионы в порядке возрастания величины стандартного электродного потенциала, т. е. чем меньше j0, тем легче ионы окисляются (S2-, I-, Вг-, Сl-). При наличии кислородсодержащих ионов на аноде окисляются молекулы воды:
2Н2О — 4е = О2 + 4Н+ (рН <, 7)
или гидроксильные ионы:
4ОН- — 4е = О2 + 2Н2О (рН>7).
Сложные кислородсодержащие ионы из водных растворов, практически, не окисляются.
На активных электродах при электролизе будет окисляться кислород.
Рассмотрим электролиз с нерастворимым анодом водных растворов солей Na2SO4 и NaCl:
а) в растворе Na2SO4 имеются ионы: Na+, SO42-, Н+, ОН-:
Na2SO4 ® 2Na+ +SO42-, H2O « Н+ + ОН- (рН = 7).
К (-) | Na2SO4, H2O | (+) А.
Na+ SO42-
Н2О Н2О
К (-): 2Н2О + 2е = Н2 + 2ОН-,
А(+):2Н2О-4е = О2 + 4Н+
Суммарной является реакция разложения воды:
2Н2О « 2Н2 + О2;
б) в растворе NaCl имеются ионы: Na+, Сl-, Н+, ОН-:
NaCl ® Na+ + Сl-, Н2О « Н+ + ОН-.
К (-): 2Н2О + 2е = Н2 + 2ОН-,
А(+):2Сl- — 2е = С12.
2Н2О + 2Сl- = Н2 + 2ОН- + С12,
2Н2О + 2NaCl = Н2 + 2NaOH + С12.
Количество вещества, подвергшегося электрохимическим превращениям, зависит от количества электричества, прошедшего через электролит. Оно определяется законами Фарадея.
Первый закон Фарадея. Масса вещества, образующегося на электроде, пропорциональна количеству пропущенного электричества:
m = k× q = k× I× t, (7.8)
где m — масса вещества, г;
k — коэффициент пропорциональности;
q — количество электричества, Кл;
I – сила тока, А;
t — время протекания тока, с.
Второй закон Фарадея. Для разряда одного моля какого-либо иона на электроде необходимо пропустить через электролит такое число фарадеев (1F = 96500 Кл/моль), которое равно числу зарядов иона.
Используя законы Фарадея, можно рассчитать массу восстанавливающегося вещества:
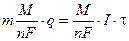 , (7.9)
, (7.9)
где М- молярная масса восстановившегося вещества, г/моль;
n — заряд иона;
F- постоянная Фарадея, 1 F = 96500 Кл/моль;
q — количество электричества, Кл;
I -сила тока, А;
t — время протекания тока, с.
Пример 2. При полном электролизе полного раствора KСl на аноде выделилось 2,8 дм3 при н. у. газа. Какие вещества и в каком количестве образовались в катодном пространстве?
Решение. В растворе КСl имеются ионы: К+, Сl-, Н+, ОН-
(КСl ® К+ + Сl-, Н2О «Н+ + OH-).
К (-): 2Н2О + 2е = Н2 + 2ОН-,
А(+):2Сl- — 2е = Сl2.
2Н2О + 2Сl- = Н2 + 2ОН- + С12,
2Н2О + 2КСl = H2 + 2КОН + Cl2.
Газ, объем которого равен 2,8 дм3, — это хлор, полученный на аноде. В катодном пространстве накапливается щелочь, КОН; кроме того, на катоде выделяется водород. Таким образом, необходимо найти n(Н2) и n(КОН).
Из уравнения: 2Н2О + 2КСl = Н2 + 2КОН + С12получаем:
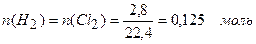
n(КОН) = 2n(Сl2) = 2× 0,125 = 0,25 моль.
Ответ: 0,125 моль Н2; 0,25 моль КОН.
Пример 3. Определите массу цинка, который выделится на катоде при электролизе раствора сульфата цинка в течение 1 ч при токе 26,8 А, если выход цинка по току равен 50 %.
Решение. Согласно закону Фарадея (7.9), подставив в уравнение числовые значения, определим массу цинка, который должен выделиться, т. е. теоретическую массу:
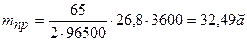
Так как выход по току цинка составляет 50 %, то практически на катоде выделится цинк массой:
mпр=32,49 × 0,5= 16,25 г.
Ответ: 16,25 г.
Пример 4. Ток силой 6 А пропускали через водный раствор серной кислоты в течение 1,5 ч. Вычислите массу разложившейся воды и объем выделившихся кислорода и водорода (условия нормальные).
Решение. Массу разложившейся воды находим из уравнения закона Фарадея, имея в виду, что 1,5 ч = 5400 с.
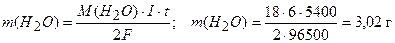 .
.
При вычислении объемов выделившихся газов (кислорода и водорода) представим уравнение закона Фарадея в следующей форме:
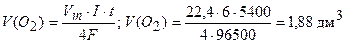
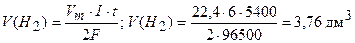
Ответ: V(O2)= 1,88 дм3; V(Н2) = 3,76 дм3.
Ваша оценка?