Рассмотрим процессы, протекающие при погружении металла в раствор собственных ионов. В узлах кристаллической решетки металла расположены ионы, находящиеся в равновесии со свободными электронами:
M+×e «M+ + e.
При погружении металла в раствор начинается сложное взаимодействие металла с компонентами раствора. В результате взаимодействия происходит окисление металла и его гидратиро-ванные ионы переходят в раствор, оставляя в металле электроны, заряд которых не скомпенсирован положительно заряженными ионами в металле:
М + тH2О = М(Н2О)mn+ + пе.
Металл становится заряженным отрицательно, а раствор -положительно. Положительно заряженные ионы из раствора притягиваются к отрицательно заряженной поверхности металла. На границе металл-раствор возникает двойной электрический слой. Между металлом и раствором возникает разность потенциалов, которая называется электродным потенциалом или потенциалом электрода. По мере перехода ионов в раствор растет отрицательный заряд поверхности металла и положительный заряд раствора, что препятствует окислению металла. Наряду с этой реакцией протекает и обратная — восстановление ионов металла до атомов:
M(H2O)mn+ + пе « М + mН2O.
С увеличением скачка потенциала между электродом и раствором скорость прямой реакции падает, а скорость обратной реакции растет. При некотором значении электродного потенциала скорость прямого процесса будет равна скорости обратного процесса, и устанавливается равновесие.
Для упрощения гидратационную воду обычно в уравнение реакции не включают и она записывается в виде:
М+ « Мn+ + пе.
Равновесие является динамическим. Процессы при равновесии идут с одинаковой скоростью в прямом и обратном направлениях. Потенциал, устанавливающийся в условиях равновесия электродной реакции, называется равновесным электродным потенциалом. Абсолютные значения электродных потенциалов экспериментально определить невозможно. Однако можно определить разность электродных потенциалов. Поэтому для характеристики электродных процессов пользуются относительными значениями электродных потенциалов. Для этого находят разность потенциалов измеряемого электрода и электрода, потенциал которого условно принимают равным нулю.
Схематически электроды записываются в виде Me/Men+, a электродный потенциал электрода — 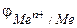 Величина электродного потенциала определяется в вольтах (В).
Величина электродного потенциала определяется в вольтах (В).
Активность металлов в окислительно-восстановительном электрохимическом процессе «металл-ион металла», а следовательно, и величины электродного потенциала, зависят от природы электродов, концентрации ионов в растворе, рН раствора, давления, температуры и определяются уравнением Нернста:
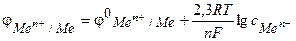 (7.1)
(7.1)
где 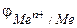 — электродный потенциал определяемого электрода, В;
— электродный потенциал определяемого электрода, В;
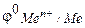 — стандартный электродный потенциал, определяемого электрода, возникающий на границе электрод-электролит при концентрации ионов в растворе, равной 1 моль/дм3, в стан дартных условиях (Т = 298 К, р = 100 кПа), В;
— стандартный электродный потенциал, определяемого электрода, возникающий на границе электрод-электролит при концентрации ионов в растворе, равной 1 моль/дм3, в стан дартных условиях (Т = 298 К, р = 100 кПа), В;
2,3 — коэффициент перевода натурального логарифма в десятичный;
R — универсальная газовая постоянная, равная 8,314 Дж/моль-К;
Т- температура, равная 298 К;
n — число электронов, участвующих в данной электродной реакции;
F- число Фарадея, равное 96500 Кл/моль;
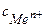 — молярная концентрация ионов в растворе электролита, моль/дм3.
— молярная концентрация ионов в растворе электролита, моль/дм3.
После подстановки значений постоянных величин уравнение Нернста (7.1) приобретает следующий вид:
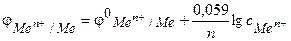 (7.2)
(7.2)
Значения стандартных электродных потенциалов (j0) определяют относительно стандартного водородного электрода, потенциал которого принят за нуль, т. е. j02H+/H2 = 0.
Металлы по величине значений их электродных потенциалов, определенных в стандартных условиях (активности в реакции металл-ион металла), располагают в электрохимический ряд напряжения.
По расположению металла в ряду активности можно судить о направленности электрохимических ОВР. Если металлы расположены в ряду далеко друг от друга, то направление реакции определяется значениями j0, если близко, то необходимо учитывать концентрацию и рН раствора.
Ваша оценка?