В растворах некоторых электролитов диссоциирует лишь часть молекул. Способность вещества к электролитической диссоциации называется степенью диссоциации. Она показывает отношение числа молекул, продиссоциированных на ионы, к общему числу молекул растворенного электролита:
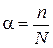 (5.1)
(5.1)
где α— степень диссоциации;
п — количество ионов в растворе;
N— общее число молекул в растворе.
По степени диссоциации в растворах все электролиты делятся на две группы. К первой группе относят электролиты, степень диссоциации которых в растворах α > 30 % и почти не зависит от концентрации раствора. Их называют сильными электролитами. К сильным электролитам в водных растворах относятся щелочи: КОН, NaOH, Ba(OH)2, Са(ОН)2; кислоты: HNO3, НСl, H2SO4, НClO4, а также их соли.
Электролиты, степень диссоциации которых в растворах α< 2 % и уменьшается с ростом концентрации, называют слабыми электролитами. К ним относят воду, ряд кислот: H2S, Н2СОз, HCN, H2Si03, органические кислоты, основания р-, d- и f-элементов и NH4OH.
Между этими двумя группами нет четкой границы, одно и то же вещество в одном растворителе проявляет свойства сильного, а в другом — слабого электролита. Например, хлорид лития и иодид натрия, имеющие ионную кристаллическую решетку, при растворении в воде ведут себя как типичные сильные электролиты, при растворении же в ацетоне или уксусной кислоте эти вещества являются слабыми электролитами со степенью диссоциации в растворах меньше единицы.
Степень диссоциации зависит:
1) от природы растворителя;
2) природы растворяемого вещества;
3) концентрации раствора (при разбавлении степень диссоциации a сильно возрастает);
4) температуры.
Пример 1. Определите количество ионов SO42- в растворе, содержащем 14,2 г сульфата натрия. Сульфат натрия диссоциирует полностью. Решение. Рассчитываем количество сульфата натрия:
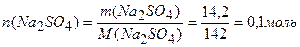
Сульфат натрия диссоциирует на ионы по уравнению:
Na2SO4 « 2Na+ + SO42-.
Согласно уравнению диссоциации определяем количество ионов SO42-, n(SO42-) = n(Na2SO4); n(SO42-) = 0,1 моль.
Ответ: n(SO42-) = 0,1 моль.
Пример 2. Степень диссоциации соляной кислоты равна 10 %. Определите количество анионов Сl- в растворе, содержащем 0,2 моль кислоты.
Решение. Рассчитаем количество кислоты, диссоциированной на ионы, в соответствии с уравнением (5.1):
п=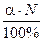 ; п =
; п =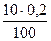 = 0,02 моль.
= 0,02 моль.
Записываем уравнение диссоциации кислоты:
НС1 = H+ + Сl-.
Согласно уравнению диссоциации, определяем количество анионовСl-: n(С1-) = n(НС1);
n(С1- ) = 0,02 моль.
Ответ: п (Сl-) = 0,02 моль.
Если степень диссоциации характеризует способность вещества распадаться на ионы, то количественной мерой процесса диссоциации является константа диссоциации.
В растворах слабых электролитов процесс диссоциации протекает обратимо и его можно представить в виде обратимой химической реакции. Так, для процесса диссоциации уксусной кислоты:
CH3COOH«CH3COO-+H+
константа равновесия этого процесса будет равна:
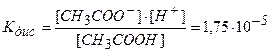 (5.2)
(5.2)
где [СНзСОО-], [Н+] — концентрация ионов;
[СН3СООН] — концентрация непродиссоциированных молекул.
Константа равновесия, соответствующая диссоциации слабого электролита, называется константой диссоциации.
Константа диссоциации зависит от природы диссоциирующего вещества и растворителя, температуры и не зависит от концентрации раствора.
Константа диссоциации показывает устойчивость молекул вещества к диссоциации. Чем меньше значение константы диссоциации в данном растворе, тем слабее диссоциирует электролит.
Степень диссоциации a изменяется с изменением концентрации раствора. Рассмотрим эту зависимость на примере слабого электролита уксусной кислоты:
CH3COOH«CH3COO-+H+.
Принимая исходную концентрацию кислоты равной с, а степень диссоциация a, получаем, что концентрация части кислоты, которая диссоциирована, будет равна aс. Так как при диссоциации одной молекулы кислоты образуется по одному иону Н+ и СНзСОО-, то их концентрации будут равны aс. Концентрация кислоты, оставшейся в недиссоциированном состоянии, будет равна с — aс = с(1 — a). Подставив значения равновесных концентраций ионов и кислоты в уравнение (5.2), получим:
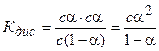 (5.3)
(5.3)
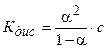
Уравнение (5.3) было получено В. Ф. Оствальдом и называется законом Оствальда. Если a<< 1, то уравнение (5.3) упрощается:
Кдис=a2×с. (5.4 а)
Откуда
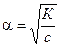 . (5.4 б)
. (5.4 б)
Уравнение (5.3) называется законом разбавления Оствальда. Из него следует, что степень диссоциации уменьшается с увеличением концентрации слабого электролита. Аналогичное уравнение можно получить для слабого основания.
Многоосновные слабые кислоты и основания диссоциируют ступенчато, причем константа диссоциации по каждой последующей ступени всегда на несколько порядков ниже, чем по предыдущей.
Зная концентрацию и степень диссоциации электролита, можно рассчитать концентрацию ионов электролита в растворе:
сi=сэл×a× k (5.5)
где сi — концентрация ионов электролита, моль/дм3;
a — степень диссоциации электролита;
сэл — концентрация электролита, моль/дм3;
k — число ионов данного вида, которое образует электролит.
Если концентрация ионов [К+] и [А-], образовавшихся в результате диссоциации, одинакова (КА « К+ + А-) и ее можно определить по уравнению [К+] = [А-] = с×a, то
[К+] = [А-] = 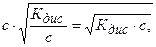 (5.6)
(5.6)
где с — концентрация раствора электролита, моль/дм3 ;
Кдис — константа диссоциации электролита.
Пример 3. Вычислите степень диссоциации хлорноватистой кислоты и концентрацию ионов водорода в растворе с молярной концентрацией 0,05 моль/дм3.
Решение. НСlO — слабый электролит: HCIO « Н+ + СlO-. Следовательно, в соответствии с законом разбавления Оствальда (5.4, б), определяем степень диссоциации:
Кдис(НСlO) = 5×10-8 моль/дм3.
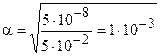
Молярную концентрацию определяем по формуле (5.5). Так как при диссоциации НС1О « Н++ СlO- образуется один ион Н+ (k(Н+) =1), то
с(Н+) = 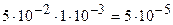 моль/дм3.
моль/дм3.
Ответ: a(HClO) = 1 ×10-3; с(Н+) = 5×10 5 моль/дм3.
Пример 4. Степень диссоциации уксусной кислоты в 0,1 моль/дм3 растворе равна 1,32×10 -2. Вычислите константу диссоциации кислоты.
Решение. В уравнение закона разбавления Оствальда (5.3) подставим данные:
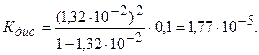
Ответ: 1,77×10-5.
Ионное произведение воды, водородный показатель (рН). Вода является слабым электролитом и диссоциирует на ионы в незначительной степени. Процесс диссоциации воды может быть записан уравнением:
НОН « Н+ + ОН-.
Константа диссоциации будет равна:
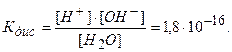
Преобразуем выражение (5.7) к следующему виду:
[Н+]-[ОН-] = Кдис[H2O]. (5.8)
Концентрацию молекул воды можно рассчитать, разделив массу 1 дм3 на массу 1 моля:
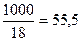 моль/дм3; Кдис =1,8×10 -16.
моль/дм3; Кдис =1,8×10 -16.
Произведение двух постоянных величин есть величина постоянная {Кдис[HгО] = const = KH20), тогда уравнение (5.8) принимает вид:
[H+]×[OH-] = KH2O. (5.9)
Полученное уравнение показывает, что для воды и разбавленных водных растворов при постоянной температуре произведение концентрации ионов водорода и гидроксила есть величина постоянная.
Эта постоянная величина называется ионным произведением воды.
Численное значение ионного произведения равно:
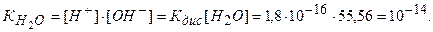 (5.10)
(5.10)
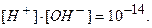
Таким образом, произведение концентрации ионов водорода и гидроксильных ионов в растворе при температуре 295 К равно 10-14.
Отсюда, для чистой воды концентрация ионов при температуре 295 К равна:
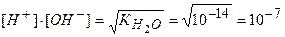 моль/дм3. (5.11)
моль/дм3. (5.11)
Если к чистой воде добавить кислоту, то часть ионов Н+ кислоты соединится с ионами ОН- и образуются молекулы воды. При этом концентрация Н+ возрастает, концентрация ОН- уменьшается, а произведение этих концентраций будет оставаться постоянным, равным 10-14 .
Допустим, что концентрация ионов водорода при добавлении кислоты увеличилась в 1000 раз и стала [Н+] = 10-4 моль/дм3, тогда концентрация ионов [ОН-] в растворе будет равна:
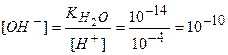 моль/дм3
моль/дм3
Мы получаем, что в растворах с различной средой всегда присутствуют ионы Н+ и ОН-.
Если: [Н+] = [ОН-] = 10 -7 — нейтральная среда;
[Н+] > [ОН-] > 10 -7 — кислая среда;
[Н+] < [ОН- ] < 10 -7 — щелочная среда.
Для характеристики кислотности (щелочности) среды введен специальный параметр — водородный показатель, или рН. Водородным показателем, или рН, называется взятый с обратным знаком десятичный логарифм концентрации ионов водорода в растворе:
pH = -lg[Н+]. (5.12)
Если [Н+] = 10 -2 моль/дм3, то рН = -lgl0 2 = 2.
Если [Н+] = 10 -7 моль/дм3, то рН = -lgl0 -7 = 7.
Если [Н+]=10 -10моль/дм3 , то рН = -lgl0 -10= 10.
Следовательно, если рН = 7 — нейтральная среда;
рН > 7 — щелочная среда;
рН < 7 — кислая среда.
Точно величину рН можно определить с помощью рН-метров, менее точно — с помощью индикаторов, которые меняют окраску в зависимости от рН.
Пример 5. Концентрация ионов водорода в растворе стала равна 4× 10 -3 моль/дм3. Определите рН раствора.
Решение. В выражение (5.12) подставляем значения:
pH = -lg(4× 10 -3) = 2,4.
Ответ: рН = 2,4.
Пример 6. Вычислите рН следующих растворов.
а) НВr с молярной концентрацией 0,02 моль/дм3;
б) NaOH с молярной концентрацией 0,2 моль/дм3.
Решение. а) НВr« Н+ + Вr-, сильный электролит. В разбавленном растворе степень диссоциации a= 1; k=1 (k — число ионов водорода, образовавшихся при диссоциации одной молекулы НВr).
Для нахождения концентрации ионов водорода воспользуемся формулой (5.5):
с(H+ )= 0,02 × 1× 1 = 0,02 моль/дм3 = 2× 10 -2 моль/дм3. Полученное значение подставляем в выражение (5.12). pH= -lg(2× 10 -2) = l,7.
б) NaOH « Na+ + ОН- — сильный электролит. В разбавленном растворе степень диссоциации а = 1.
Для нахождения концентрации гидроксид-ионов используем формулу (5.5):
с(ОН- )= 0,2× 1× 1 =0,2 моль/дм3 = 2× 10 -1моль/дм3.
Подставляем значения:
pOH = -lg(2× 10-1) = 0,7; pH = 14 — 0,7= 13,3.
Ответ: а) рН = 1,7; б) рН =13,3.
Пример 7. Вычислите рН раствора хлорноватистой кислоты с молярной концентрацией 0,05 моль/дм3 (Kдис(НСlO) = 5× 10 -8 моль/дм3).
Решение. НС1О — слабый электролит:
HClO«H++ClO- .
Следовательно, в соответствии с законом разбавления Оствальда (5.4, б) определяем степень диссоциации:
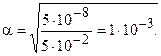
k(H+)=1
Молярную концентрацию ионов водорода определяем по формуле (5.5):
c(H+)=5×10-2 ×1×10-3 ×1=5×10-5 моль/дм3.
Полученное значение подставляем в выражение (5.12): pH = -lg(5 ×10 5) =4,3.
Ответ: рН = 4,3.
Ваша оценка?