Условие химического равновесия. Для любого химического процесса при некоторой температуре энтальпийный и энтропийный факторы уравниваются. Две противоположные тенденции уравновешивают друг друга, т. е. DН= TDS. В этом случае соблюдается уравнение:
DrG° = DrH ° — TDrS ° = 0,
которое является термодинамическим условием химического равновесия.
Химическое равновесие имеет динамический характер. Когда скорость реакции в прямом направлении равна скорости реакции в обратном направлении, наступает состояние химического равновесия. В условиях химического равновесия концентрации исходных веществ и продуктов реакции не изменяются во времени называются равновесными концентрациями веществ. В дальнейшем равновесные концентрации будем обозначать символом вещества в квадратных скобках. Например, равновесные концентрации водорода и аммиака будут обозначаться [Н2] и [NH3].
Константа химического равновесия. При равновесии химической реакции:
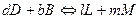
энергия Гиббса равна:
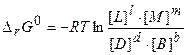 (3.12)
(3.12)
где [L], [M],, [D], [В] — равновесные концентрации соответствующих веществ;
l, m, d, b — показатели степени, равные стехиометрическим коэффициентам.
Отношение 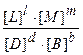 получило название константы химического равновесия (Кр):
получило название константы химического равновесия (Кр):
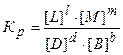 (3.13)
(3.13)
Это уравнение является вариантом математического выражения закона действующих масс. Для обратимых химических реакций закон действующих масс может быть сформулирован в следующем виде: отношение произведения равновесных концентраций продуктов реакции в степенях, равных стехиометрическим коэффициентам, к произведению равновесных концентраций исходных веществ в степенях, равных стехиометрическим коэффициентам, при Т = const, является величиной постоянной.
Например, для реакции синтеза аммиака:
N2 + ЗН2 = 2NH3; 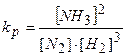 .
.
Чем больше константа равновесия, тем «глубже» протекает реакция, т. е. тем больше выход продуктов реакции.
Для гетерогенных химических реакций в выражение константы равновесия, как и в уравнение закона действующих масс входят концентрации только тех веществ, которые находятся газовой фазе или в растворе. Концентрация вещества, находящегося в твердой фазе, обычно постоянна.
Катализатор не влияет на значение константы равновесия поскольку он одинаково снижает энергию активации прямой и обратной реакции и поэтому одинаково изменяет их скорости Катализатор лишь ускоряет достижение химического равновесия, но не влияет на количественный выход продуктов реакции.
Пример 11. Для реакции синтеза аммиака
N2(r) + 3H2(r)«2NH3(r)
равновесные концентрации N2, Н2 и NH3 равны соответственно 3 моль/дм3, 2 моль/дм3 и 0,3 моль/дм3. Найдите исходные концентрации N2 и Н2 и константу равновесия реакции.
Решение. Пусть объем системы равен 1 дм» и в холе реакции q изменяется. Обозначим равновесные концентрации как [H2], [N2], [NH3], исходные — как с(Н2), c(N2), концентрации и количество прореагировавшего вещества — с(Н2)прор c(N2)прор. n(N2)прор и n(Н2)прор.
с(Н2) = [Н2] + с(H2)поор;
c(N2) = [N2]+ c(N1)w.
Находим количество прореагировавшего азота n(N2)прор и вoдopoд n(Н2)прор. по количеству образовавшегося аммиака. Составляем пропорции согласно уравнениям реакций: i
на образование 2 моль NH3 расходуется 1 моль N2, i
на образование 0,3 моль NH3 расходуется х моль N2.
Отсюда х = 0,15 моль — количество прореагировавшего азота n(N2)прор=0,15 моль.
Находим концентрацию прореагировавшего N2:
c(N2) = 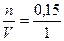 = 0,15 моль/дм3 I
= 0,15 моль/дм3 I
Аналогично определяем количество прореагировавшего водород на образование 2 моль NH3 расходуется 3 моль Н2, на образование 0,3 моль NH3 расходуется y моль Н2.
Отсюда у = 0,45 моль, л(Н2)прор = 0,45 моль. Находим концентрацию прореагировавшего Н2:
с(Н2) = 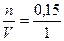 = 0,45 моль/дм3.
= 0,45 моль/дм3.
Следовательно, исходные концентрации азота и водорода равны:
с(Н2) = [Н2] + c(H2)прор = 3 + 0,15 = 3,15 моль/лм3;
c(N2) = [N2] + c(N2)прор = 2 + 0,45 = 2,45 моль/дм3.
Находим константу равновесия, используя выражение (3.13):
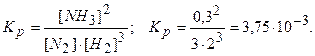
Ответ: с(Н2) = 3,15 моль; c(N2) = 2,45 моль; Кр = 3,75×10 -3. Подставляя константу равновесия в уравнение (3.12), получаем:
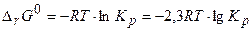 (3.14)
(3.14)
При температуре 298 К
DrG0298 = -5,71×lgKp298 = -2,48×lnKp 298.
Уравнение (3.14) можно записать в виде:
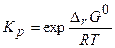 (3.15)
(3.15)
Рассчитав величину DrG0 химической реакции, можно определить константу химического равновесия. Следует отметить, то DrG0 < 0 только в случае, когда lgKp > 0, т. е. Кp > 1; DrG0 > 0, когда lgKp < 0, т. е. Кp < 1. При DrG0 < 0 равновесие смещено в направлении прямой реакции и выход продуктов реакции сравнительно велик, при DrG0 > 0 равновесие смещено в сторону обратной реакции.
Случай, когда Кр = 1 соответствует минимуму энергии Гиббса, т. е. DrG0 = 0, тогда из выражения DrG0 = DrН0 — ТDrS0 можно определить температуру, при которой Кp= 1 (уравнение (2.18)):
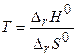 (2.20)
(2.20)
Принцип Ле Шателье. При внешнем воздействии на систему происходит смещение химического равновесия, т. е. изменяются равновесные концентрации исходных веществ и продуктов реакции.
Характер смещения равновесия под влиянием внешних воз действий можно прогнозировать, применяя принцип Ле Шателье: если на систему, находящуюся в равновесии, оказывается внешнее воздействие, то в результате протекающих в ней процессов равновесие смещается в таком направлении, которое ослабляет внешнее воздействие.
Химическое равновесие может смещаться при изменении температуры, давления или концентрации:
1)при увеличении температуры равновесие смещается в сторону эндотермического процесса, при понижении температуры — в сторону экзотермического процесса;
2) при увеличении давления (уменьшении объема системы равновесие смещается в гу сторону, где содержится меньшее количество молекул газообразных веществ; при понижении давления (увеличении объема системы) — в сторону большего количества молекул. Если количество молекул газов в обеих часта уравнения одинаково, то изменение давления не влияет на смещение равновесия;
3) при увеличении концентрации реагентов равновесие смещается в сторону прямой реакции, при увеличении концентрации продуктов — в сторону обратной реакции.
Введение катализатора не влияет на смещение равновесия поскольку в равной мере изменяет скорость как прямой, так и обратной реакции.
Пример 12. Какое влияние на состояние равновесия реакции
S(k)+O2(г)«SO2(г)+Q
окажут: а) повышение температуры; б) увеличение давления; в) введение дополнительной порции серы или кислорода; г) введение в систем; катализатора?
Решение. Повышение температуры сместит равновесие влево, и сторону эндотермической реакции.
Поскольку количества молекул газов в обеих частях уравнения равны (по 1 моль), то изменение давления не влияет на смешение равновесия.
Изменение концентрации серы (твердое вещество) также не изменит равновесие, а увеличение концентрации кислорода сместит равновесие вправо: быстрее пойдет прямая реакция, в которой кислород расходуется.
Так как катализатор в равной мере ускоряет как прямую, так и обратную реакцию, то введение его в систему не приводит к смещению химического равновесия.
Ваша оценка?