Закон Гесса: тепловой эффект реакции, протекающей при постоянном давлении и (или) объеме, зависит от природы и состояния исходных веществ и конечных продуктов, но не зависит от пути реакции.
Закон Гесса лежит в основе термохимических расчетов. Проиллюстрируем закон Гесса на примере реакции сгорания метана:
СH4 + 2О2 = СО2 + 2Н2О (г), DrH0 =-802,34 кДж.
Эту же реакцию можно провести через стадию образования СО:
СН4+ 3/2О2 = СО + 2Н2О (г), А,}?2 = -519,33 кДж,
СО + 1/2 О2 = СО2, ДГД°3 = -283,01 кДж,
DrH01 = DrH0 2+ DrH0 з = (-519,33) кДж + (-283,01) кДж =
= -802,34 кДж.
Следствие из закона Гесса: энтальпия химических реакций равна сумме энтальпий образования продуктов реакций за вычетом суммы энтальпий образования исходных веществ с учетом их стехиометрических коэффициентов.
В результате протекания реакции
bВ + dD=lL + mM (2.13)
ее тепловой эффект рассчитывается по формуле:
DrH°1 = lDfH°L + mDfH°M — dDfH°D -bDfH°B. (2.14)
Стехиометрические коэффициенты в уравнениях реакций показывают, в каких количественных соотношениях находятся реагенты и продукты реакции на микро- и макроуровнях: на микроуровне соотношения между молекулами веществ, на макроуровне — между химическими количествами веществ.
Пример 1. Определите тепловой эффект реакции получения водорода из природного газа:
СН4 + 2Н2О (г) = СО2 + 4Н2.
Решение. DrН°=D/Н°CОг -DfH°CH4 -2DfH0H2O
Подставляя значения величин энтальпий образования (приложение Б) (в кДж/моль), получаем:
DrН° = 1 моль(-393,51 кДж/моль)- 1 моль(-74,85 кДж/моль)-
— 2 моль (241,82 кДж/моль) = 164,98 кДж.
Ответ: DrН° = 164,98 кДж.
Можно также рассчитать значение энтальпии образования одного из исходных веществ или продуктов реакции, если известны энтальпии образования остальных реагентов и энтальпия химической реакции. Например, энтальпию образования вещества М в уравнении (2.13) можно определить по видоизмененному уравнению (2.14):
DfH°M=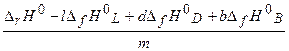 .
.
Пример 2. Рассчитайте стандартную энтальпию образования пропана С3Н8, если стандартная энтальпия реакции его сгорания равна DrН° = -2043,86 кДж.
Решение. С3Н8 + 5О2 = ЗСО2 + 4Н2О (г).
В соответствии с уравнением (2.14) запишем:
DfН°C3H4=3D/Н°CОг +4DfH°H2O® -DrH0.
Подставив значение DfН° и справочные данные из приложения Б, получим:
DfН°C3H4=3моль (-393,51 кДж/моль) +
+ 4 моль (- 241,82 кДж/моль) — (2043,86 кДж)/ моль =
= -103,85 кДж/моль.
Ответ: DfН°C3H4 =-103,85 кДж/моль.
Таким образом, зная энтальпии образования продуктов реакции и исходных веществ, можно, используя закон Гесса и его следствие, рассчитать энтальпию химической реакции.
Теплота сгорания вещества. Тепловой эффект реакции окисления I моль вещества с образованием высших оксидов входящих в него элементов называется теплотой сгорания этого вещества DСН°
Расчет теплоты сгорания, как и любого теплового эффекта, проводится с использованием закона Гесса.
Пример 3. Рассчитайте теплоту сгорания этанола при температуре 298 К:
Решение. С2Н5ОН (ж) + ЗО2 = 2СО2 + ЗН2О (г).
В соответствии с уравнением (2.14):
DСН°C2Н5ОН=2DfН°CО2+3DfН°Н2О®-DfН°C2Н5ОН
Подставляя данные DfН°из приложения Б, получаем стандартную теплоту сгорания этанола:
Ответ: DСН°с2н5он =-1234,7 кДж
Удельная теплота сгорания пищи получила название калорийность.
Ваша оценка?