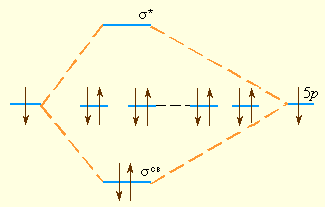
Водород, помимо наиболее стабильной молекулы 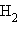 и сольватированного иона H+ существует в атомарном состоянии, в виде иона
и сольватированного иона H+ существует в атомарном состоянии, в виде иона 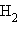 , молекулярных ионов
, молекулярных ионов 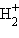 и
и 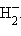 Из-за малого радиуса атома энергия связи в молекуле водорода наибольшая из всех атомных гомонуклеарных молекул VIIА и IА групп:
Из-за малого радиуса атома энергия связи в молекуле водорода наибольшая из всех атомных гомонуклеарных молекул VIIА и IА групп:
| ||||||||||||||||||
| Таблица 8.2. |
Образование иона H+ сопровождается резким уменьшением эффективного радиуса, изменением кислотно-основных свойств и окислительно-восстановительных потенциалов некоторых соединений в присутствии H+, гидратированием в водных растворах протона с образованием иона гидроксония H3O+. Вакантность 1s-орбитали способствует образованию водородной связи.
Водород следует рассматривать как не имеющий полных аналогов химический элемент, поэтому его помещают либо в первую, либо в седьмую группу. К группе галогенов водород можно отнести из-за легкой замещаемости водорода галогенами в органических соединениях и способности к образованию аниона H– (гидрид-иона).
|
|
| Рисунок 8.2. Воздушные шары надувают гелием. |
Соединения водорода с менее электроотрицательными элементами называют гидридами. Промежуточное значение ЭО (2,1) позволяет водороду образовывать химические соединения с различной степенью полярности химической связи, поэтому их классифицируют следующим образом: ионные (солеобразные) соединения (с s-элементами), ковалентно-полярные (с p-элементами), металлоподобные фазы внедрения (с переходными металлами) (табл. 8.1).
Переход от одного типа соединений к другому совершается постепенно. Так, гидриды меди и цинка занимают промежуточное положение между ионными и ковалентными, а гидриды серебра и золота сходны с гидридами переходных металлов.
Более подробно соединения с водородом будут расмотрены в обзорах соответствующих элементов.
Второй элемент первого периода – гелий – формально входит в VIIIА подгруппу. Гелий – типичный инертный элемент, его неспособность вступать в химическое взаимодействие с другими элементами предопределена устойчивостью его электронной конфигурации 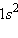 . К типично химическим соединениям можно отнести лишь молекулярный ион
. К типично химическим соединениям можно отнести лишь молекулярный ион 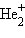 и гидрид гелия HeH с электронной формулой
и гидрид гелия HeH с электронной формулой 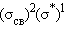 и кратностью связи 0,5.
и кратностью связи 0,5.
Ваша оценка?