Строение периодической системы элементов строго соответствует строению атомов химических элементов. Основные закономерности:
1. Порядковый номер элемента равен заряду ядра атома и общему числу  в атоме.
в атоме.
2. Номер периода определяет число энергетических уровней в атоме элемента данного периода, на которых имеются  .
.
3. Номер группы определяет максимально возможное число валентных  . Каждая группа подразделяется на две подгруппы – главную и побочную. Если элемент принадлежит к главной подгруппе, то число
. Каждая группа подразделяется на две подгруппы – главную и побочную. Если элемент принадлежит к главной подгруппе, то число  на внешнем уровне равно номеру группы. Если элемент принадлежит к побочной подгруппе, то число
на внешнем уровне равно номеру группы. Если элемент принадлежит к побочной подгруппе, то число  на внешнем уровне, как правило, равно 2. У некоторых элементов происходит провал
на внешнем уровне, как правило, равно 2. У некоторых элементов происходит провал  с внешнего на предвнешний уровень – Cr, Cu, Ag, Au, Pt и др., т.е. на внешнем уровне находится 1
с внешнего на предвнешний уровень – Cr, Cu, Ag, Au, Pt и др., т.е. на внешнем уровне находится 1 , а другой переходит на предвнешний уровень.
, а другой переходит на предвнешний уровень.
4. Электронное семейство. Все элементы периодической системы принадлежат к четырем электронным семействам s, p, d, f. Это определяется тем, какой подуровень элемента заполняется электронами последним. Любой период начинается с заполнения s-подуровня, поэтому первые два элемента принадлежат к s-семейству. Последние шесть элементов каждого периода принадлежат к р-семейству. В побочных подгруппах находятся d и f-элементы.
Зная порядковый номер элемента, можно написать электронную формулу атома – распределение всех имеющихся в атоме  по энергетическим уровням и орбиталям. Кроме электронной формулы составляют электронно-графические формулы.
по энергетическим уровням и орбиталям. Кроме электронной формулы составляют электронно-графические формулы.
Пример 1. Составить электронную формулу элемента №51. Для электронов внешнего уровня написать электронно-графическую формулу.
Решение. По таблице периодической системы Д.И.Менделеева находим элемент №51 – это сурьма. Атом имеет заряд ядра +51 и на его энергетических уровнях находится 51 электрон.
Период 5, следовательно  распределены на пяти энергетических уровнях.
распределены на пяти энергетических уровнях.
Группа V, значит максимально возможное число валентных  равно пяти.
равно пяти.
Подгруппа главная, следовательно валентные  находятся на внешнем уровне, и сурьма принадлежит к р-семейству.
находятся на внешнем уровне, и сурьма принадлежит к р-семейству.
Электронная формула:
Sb +51 1s22s22p63s23p64s23d104p65s24d105p3
Электронно-графическая формула:
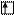
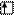
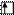
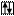 5
5
s p
Пример 2. Строение внешнего и предвнешнего энергетических уровней выражается формулой 3d34s2. Какой это элемент? Написать электронно-графическую формулу для этого состояния.
Решение. Главное квантовое число n=4, это значит, что элемент находится в четвертом периоде. На внешнем и предвнешнем энергетических уровнях находится 5 валентных  , это значит, что элемент находится в пятой группе. Так как у элемента идет заполнение d-подуровня, значит он относится к d-элементам и расположен в побочной подгруппе. Искомый элемент – ванадий.
, это значит, что элемент находится в пятой группе. Так как у элемента идет заполнение d-подуровня, значит он относится к d-элементам и расположен в побочной подгруппе. Искомый элемент – ванадий.


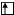
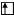
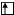
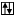 Электронно-графическая формула: 3 4
Электронно-графическая формула: 3 4
d s
Взаимосвязь электронного строения атома со свойствами простых и сложных веществ. Комплементарность
Валентность элемента. По квантово-механическим представлениям валентность элемента определяется числом неспаренных электронов в атоме элемента.
Валентные электроны могут принимать участие в образовании химических связей: для s- и р-элементов валентными являются электроны внешнего энергетического уровня, для d-семейства – электроны внешнего и предвнешнего энергетических уровней.
Например, валентными электронами в атоме селена считаются …4s24p4. В нормальном состоянии атома эти  распределены по соответствующим орбиталям следующим образом:
распределены по соответствующим орбиталям следующим образом:





 Se B=2
Se B=2
4s 4p 4d
По этой схеме неспаренных электронов два, следовательно, валентность селена в нормальном состоянии атома равна двум.
Если атому сообщить некоторое количество энергии, то атом перейдет в так называемое возбужденное состояние за счет перехода одного или нескольких из спаренных электронов в свободные орбитали данного энергетического уровня. Например,
 |




 Se* B*=4
Se* B*=4
4s 4p 4d
 В этом энергетическом состоянии (…4s24p34d1) неспаренных электронов четыре, следовательно, валентность равна четырем.
В этом энергетическом состоянии (…4s24p34d1) неспаренных электронов четыре, следовательно, валентность равна четырем.



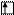 Se** B**=6
Se** B**=6
4s 4p 4d
В данном энергетическом состоянии (…4s14p34d2) шесть неспаренных  , следовательно, валентность селена равна шести.
, следовательно, валентность селена равна шести.
 Для элементов побочных подгрупп валентность атомов в нормальном состоянии равна нулю, т.к. внешние спаренные s-электроны как бы блокируют неспаренные d-электроны. Например, в атоме ванадия валентными
Для элементов побочных подгрупп валентность атомов в нормальном состоянии равна нулю, т.к. внешние спаренные s-электроны как бы блокируют неспаренные d-электроны. Например, в атоме ванадия валентными  считаются …3d34s2. В нормальном состоянии:
считаются …3d34s2. В нормальном состоянии:










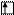
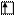
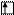 V B=0
V B=0
3d 4s 4p 4d
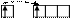 | |||||
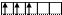 | |||||
 |
V* B*=5
3d 4s 4p 4d
Для элементов побочных подгрупп можно определить только максимальную валентность в возбужденном состоянии атома.
Степень окисления элемента. Степень окисления элемента часто совпадает по абсолютному значению с валентностью этого элемента в определенном энергетическом состоянии. Для элемента, имеющего переменную валентность, характерны и переменные степени окисления. Например, для хлора.
Внешний энергетический Валентность Степени окисления
уровень атома хлора хлора хлора





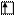
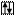
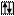
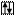 Cl B=1 -1; +1
Cl B=1 -1; +1
3s 3p 3d
 |




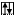
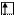
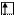 Cl* B*=3 +3
Cl* B*=3 +3
3s 3p 3d
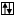 | 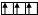 |  | |||
 Cl** B**=5 +5
Cl** B**=5 +5
3s 3p 3d


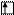
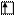
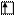
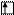
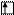 Cl*** B***=7 +7
Cl*** B***=7 +7
3s 3p 3d
Металлические свойства проявляют элементы, на высшем энергетическом уровне которых число  меньше номера внешнего энергетического уровня. Это все d- и f-элементы, s-элементы (кроме водорода и гелия), некоторые р-элементы.
меньше номера внешнего энергетического уровня. Это все d- и f-элементы, s-элементы (кроме водорода и гелия), некоторые р-элементы.
Неметаллические свойства проявляют элементы, у атомов которых на внешнем энергетическом уровне число  больше номера этого уровня.
больше номера этого уровня.
Если число  внешнего энергетического уровня совпадает с номером уровня, то свойства элемента промежуточные между свойствами металлов и неметаллов.
внешнего энергетического уровня совпадает с номером уровня, то свойства элемента промежуточные между свойствами металлов и неметаллов.
Свойства оксидов и гидроксидов. Кислотно-основные свойства оксидов и гидроксидов зависят от степени окисления элементов.
Оксиды металлов в низших степенях окисления (+1, +2) имеют основный характер. В качестве гидроксидов им соответствуют основания:
Основный оксид Гидроксид-основание
Na2O NaOH
MgO Mg(OH)2
MnO Mn(OH)2
Оксиды неметаллов и металлов со степенью окисления больше +4 имеют кислотный характер. В качестве гидроксидов кислотным оксидам соответствуют кислоты:
Кислотный оксид Гидроксид-кислота
SO3 H2SO4
N2O5 HNO3
Cl2O7 HClO4
CrO3 H2CrO4
Mn2O7 HMnO4
Оксиды металлов в степени окисления +3, +4 проявляют, как правило, амфотерные свойства. Амфотерными свойствами обладают также оксиды некоторых металлов в степени окисления +2: BеO, ZnO, PbO, SnO, CuO. В качестве гидроксидов амфотерным оксидам соответствуют и кислоты, и основания одновременно.
Кислота Амфотерный оксид Основание
H2ZnO2 ZnO Zn(OH)2
HAlO2 Al2O3 Al(OH)3
H2SnO3 SnO2 Sn(OH)4
Пример 1. Порядковый номер элемента равен 30. Укажите положение элемента в периодической системе: период, группу, подгруппу. Составьте электронную формулу атома элемента. Укажите электронное семейство, металл или неметалл. Составьте электронно-графическую формулу для валентных электронов в нормальном и возбужденном состояниях. Укажите возможные валентности и степени окисления атома. Составьте формулы высших и низших оксидов и соответствующих им гидроксидов.
Решение. В периодической системе элементов Д.И.Менделеева находим элемент с порядковым номером 30 – цинк: период – 4, группа – II, подгруппа – побочная . Заряд ядра составляет +30, число электронов – 30.
Электронная формула атома цинка:
1s22s22p63s24s23d10.
Цинк относится к d-семейству, т.к. последним заполняется d-подуровень. Число  на внешнем уровне (2) меньше номера внешнего уровня (4), следовательно, элемент – металл.
на внешнем уровне (2) меньше номера внешнего уровня (4), следовательно, элемент – металл.
Электронно-графическая формула для энергетического состояния атома …4s23d10
а) в нормальном состоянии








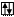
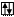
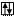
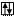
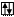
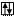 Zn B=0
Zn B=0
3d 4s 4p 4d
б) в возбужденном состоянии
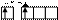 | |||||
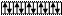 | |||||
 | |||||
Zn* B*=2
3d 4s 4p 4d
В соединениях цинк имеет степень окисления +2.
Оксид ZnO. Характер оксида амфотерный.
Гидроксид Zn(OH)2 и H2ZnO2.
Пример 2. Окончание электронной формулы …5s25p3. Укажите положение элемента в периодической системе: период, группу, подгруппу, назвать элемент. Составьте электронную формулу атома элемента. Укажите электронное семейство, металл или неметалл. Составьте электронно-графическую формулу для валентных  в нормальном и возбужденном состояниях. Укажите возможные валентности и степени окисления атома. Составьте формулы высших и низших оксидов и соответствующих им гидроксидов.
в нормальном и возбужденном состояниях. Укажите возможные валентности и степени окисления атома. Составьте формулы высших и низших оксидов и соответствующих им гидроксидов.
Решение. Так как внешний энергетический уровень атома пятый, элемент находится в пятом периоде. Общее число валентных  равно пяти, следовательно, элемент находится в пятой группе. Так как заполняется р-подуровень, то элемент расположен в главной подгруппе. В таблице элементов Д.И.Менделеева находим, что это элемент №51 – сурьма. Заряд ядра равен +51, общее число
равно пяти, следовательно, элемент находится в пятой группе. Так как заполняется р-подуровень, то элемент расположен в главной подгруппе. В таблице элементов Д.И.Менделеева находим, что это элемент №51 – сурьма. Заряд ядра равен +51, общее число  — 51. Сурьма относится к р-семейству, т.к. последним заполняется р-подуровень. Число
— 51. Сурьма относится к р-семейству, т.к. последним заполняется р-подуровень. Число  на внешнем энергетическом уровне (5) равно числу внешнего уровня (5), это значит, что сурьма может проявлять как металлические, так и неметаллические свойства.
на внешнем энергетическом уровне (5) равно числу внешнего уровня (5), это значит, что сурьма может проявлять как металлические, так и неметаллические свойства.
Электронная формула атома сурьмы:
1s22s22p63s23p64s23d104p65s24d105p3.
Электронно-графическая формула:
а) в нормальном состоянии




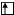
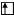
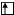
 Sb B=3
Sb B=3
5s 5p 5d
б) в возбужденном состоянии







 Sb* B*=3
Sb* B*=3
5s 5p 5d
Степени окисления сурьмы в соединениях: +3, +5.
Оксид Sb2O3.
Характер оксида амфотерный.
Гидроксиды Sb(OH)3 и HSbO2.
Высший оксид Sb2O5.
Характер оксида кислотный.
Гидроксид HSbO3.
Ваша оценка?







